Embriyoların döllenme evresinden blastosist (beşinci gün embriyosu) oluşumuna kadar sürekli takip edildikleri sistemlerin geliştirilmesi embriyoyu oluşturan her bir blastomer hücresinin ne zaman bölündüğünün tespit edilmesini sağlamıştır. Klasik morfolojik (şekil incelenerek yapılan) değerlendirmede...
Kasım 2013
Sürekli Embriyo İzleme (Time-lapse Imaging) sistemlerinin IVF laboratuvarlarında embriyo kültürü amaçlı kullanımı sayesinde embriyoların döllenme evresinden sonraki tüm gelişim sürecinin kaydedilmesi ve incelenebilmesi mümkün hale gelmiştir.
Klasik embriyo değerlendirmede (morfolojik-şekilsel değerlendirme), embriyolar kısa süreliğine bulundukları inkübatörlerden çıkarılarak mikroskop ile değerlendirmeleri yapılmaktadır. Fakat bu durum hem kültür inkübatörünün iç ortamının bozulmasına, hem de embriyonun, gelişimi için uygun olmayan, dış ortam şartlarına maruz kalmasına sebep olmaktadır. Sürekli Embriyo İzleme Sistemlerinde ise sistem içerisinde mevcut olan hareketli mikroskop ve kamera ile embriyoların görüntüleri belirli aralıklarla kaydedilmekte, böylece değerlendirme için embriyoların inkübatörden çıkarılmasına gerek kalmamaktadır. (Şekil 1).
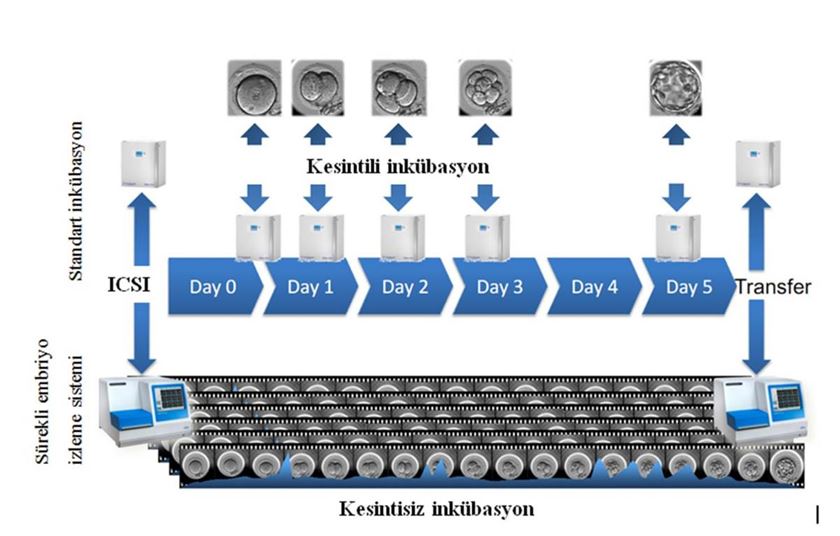 |
| Şekil 1: Kesintili ve kesintisiz inkübasyon |
Bu sistemler ile hücre bölünme zamanları, fragman (hücre parçacığı) oluşumu ve emilimi, multinükleasyon (hücre içerisinde birden fazla çekirdek gözlenmesi), düzensiz bölünme ve blastosist oluşum zamanı gözlemlenebilmektedir. Özetle, embriyo değerlendirmesi ve seçimi standart inkübatör sistemlerinde sadece anlık morfolojik değerlendirmeyle kısıtlanmışken, Sürekli Embriyo İzleme Sistemlerinde morfolojiyle ilgili ek birçok parametreyle birlikte zaman bilgisi de eklenerek “morfo-kinetik” olarak tanımlanan daha gelişmiş bir değerlendirme yapılabilmektedir.
Sürekli Embriyo İzleme Sisteminde inkübe edilen ve embriyo gelişiminin 3. gününde transfer edilen embriyoların, hem morfolojik özelliklerinin hem de bölünme zamanlarının değerlendirilmesi sonucunda, gebelik sonucunu tahmin etmeye yönelik bir model oluşturulması sağlanmıştır (Meseguer et al., 2011). Bu çalışmada, sırasıyla;
embriyonun gebelik oluşturma potansiyeli ile bağlantılı bulunmuştur. Takip eden bir başka çalışmada ise oluşturulan model, blastosist oluşturma potansiyeli ve kalitesi ile de ilişkilendirilmiştir (Cruz et al., 2012). Araştırmacılar, embriyoların Sürekli Embriyo İzleme Sistemlerinde gelişmesi ve seçilmesi halinde klinik gebelik oranındaki artışın %9 olacağını göstermişlerdir (Meseguer et al., 2012).
Sürekli Embriyo İzleme Sistemleri hücre döngülerinin detaylı incelemesini ve kesin zamanlamalarının belirlenmesini sağladığı için direkt klivaj gibi bölünme anomalilerinin de gözlemlenebilmesini sağlamıştır. Direkt klivaj bir hücrenin iki hücreye bölünmesi yerine anormal olarak üç hücreye bölünmesini tarif etmektedir (Şekil 2).
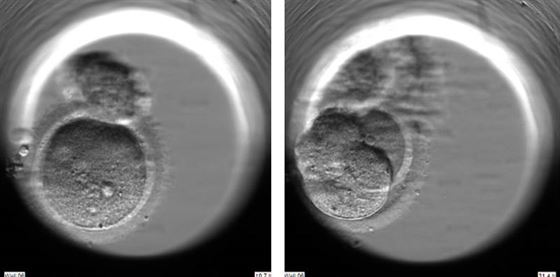 |
| Şekil 2: Döllenmiş yumurta iki hücreye bölünmek yerine üç hücreye bölünüyor |
İki hücreden üç hücreye 5 saatten kısa bir sürede bölünmüş olan embriyoların tutunma oranlarının normal bölünmelere sahip embriyolara kıyasla anlamlı olarak daha düşük olduğu çok merkezli bir çalışmada gösterilmiştir (5 saat altı %1.2 / 5 saat üstü %20.2). Dolayısıyla, direkt klivaj bulgusu olan embriyoların transferi ancak seçilebilecek başka embriyo bulunmaması halinde düşünülmelidir (Rubio et al., 2012).
Embriyoların kromozom sayısı yönünden tanımlanması son yıllarda yaşanan teknolojik gelişmeler ile kolaylaşmış ve embriyolojik verilerin genetik ile birleştirilmesinin önünü açarak tüp bebek alanında çığır açmıştır. Bu konuyla ilişkili yeni bir bilimsel çalışma embriyonun kromozom sayısını, blastülasyon (blastosist kavitesinin oluşumu) ve tam blastosist olma zamanları ile ilişkilendirmiş ve anöploidi (kromozom sayısında anormallik) riskini belirlemeye yönelik bir model oluşturmuştur (Campbell et al., 2013 a). Bu anöploidi risk modeli kullanılarak, biyopsi uygulanmamış embriyolar arasında seçim yapılan bir çalışmada, düşük risk taşıdığı tanımlanan embriyoların transferiyle, canlı doğum oranlarında istatistik olarak anlamlı seviyede daha iyi sonuçlar elde edilmiştir. (Campbell et al., 2013 b). Merkezimizde de konuyla ilgili çalışmalar devam etmekte ve bilimsel çalışmalardaki bulgular ve bizim bulgularımız dikkatle incelenerek, uygun bulunanlar embriyo seçimini iyileştirmek amacıyla kullanılmaktadır. Güncel bulgularımıza göre, gelişiminin ilk 3 gününde senkronize hücre bölünmesi gösteren blastosistlerin transferiyle anlamlı seviyede daha iyi gebelik sonuçları elde edildiği gözlenmiştir.
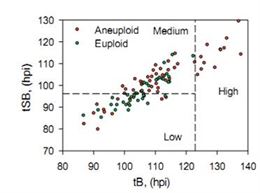 |
| Şekil 3: Campbell’in risk modeli |
Campbell, A., Fishel, S., Bowman, N., Duffy, S., Sedler, M., Hickman, C.F., Modelling a risk classification of aneuploidy in human embryos using non-invasive morphokinetics. Reprod.Biomed.Online, 2013 a; 26: 477-485.
Campbell, A., Fishel, S., Bowman, N., Duffy, S., Sedler, M., Thornton, S., Retrospective analysis of outcomes after IVF using an aneuploidy risk model derived from time-lapse imaging without PGS. Reprod.Biomed.Online, 2013 b; doi:pii: S1472-6483(13)00238-1. 10.1016/j.rbmo.2013.04.013.
Cruz M., Garrido, N., Herrero, J., Pérez-Cano, I., Muñoz, M., Meseguer, M., Timing of cell division in human cleavage-stage embryos is linked with blastocyst formation and quality. Reprod.Biomed. Online, 2012; 25: 371-381.
Meseguer, M., Herrero, J., Tejera, A., Hilligsoe, K.M., Ramsing, N.B., Remohi, J., The use of morphokinetics as a predictor of embryo implantation. Hum.Reprod, 2011; 26: 2658–2671.
Meseguer, M., Rubio, I., Cruz, M., Basile, N., Marcos, J., Requena, A., Embryo incubation and selection in a time-lapse monitoring system improves pregnancy outcome compared with a standard incubator: a retrospective cohort study. Fertil.Steril, 2012; 98: 1481–1489.
Daha detaylı bilgi için,
Bio. Caroline Pirkevi (caroline.pirkevi@memorial.com.tr)