Memorial Şişli Hastanesi, IVF Laboratuvarı, 20 yılı aşkın süredir çocuk sahibi olmaya çalışan çiftlere umut kaynağı olmaktadır. Laboratuvarımız Androloji ve Embriyoloji bölümlerinden oluşmaktadır.
Merkezimizde özel sperm seçme yöntemleri, mikroenjeksiyon, yumurtaların kimyasal veya elektrik aktivasyonu ile uyarılması, embriyoların kamera yardımı ile sürekli izlenmesi sistemi (Timelapse Imaging Systems), embriyo zarının inceltilmesi (assisted hatching), embriyoların ileri döneme kültüre edilmesi (blastokist kültürü), oosit-embriyo dondurulması (vitrifikasyon tekniği ile), genetik tanı amaçlı embriyo (trofektoderm) biyopsisi gibi ileri laboratuvar teknikleri kullanılarak hizmet verilmektedir. Mikroenjeksiyon, TESE, TESA, embriyo dondurma, preimplantasyon genetik tanı gibi birçok yöntem ülkemizde ilk olarak Prof. Dr. Semra Kahraman ve ekibi tarafından uygulanmıştır. 2003 yılında ise ilk kez embriyonik kök hücrelerden insan embriyonik kök hücre dizileri elde edilmiştir.
Tüp Bebek Laboratuvarları için oluşturulmuş ISO 15189 belgesini 2011 yılında almaya hak kazanan laboratuvarımız bugüne kadar ülkemizde bu belgeyi alan ilk ve tek laboratuvar olma ünvanına sahiptir. Ayrıca laboratuvarda hasta güvenliği ve embriyoların karışmasını engellemek için tüm aşamaları elektronik olarak kontrol eden radyofrekans tabanlı RI Witness sistemi kullanılmaktadır.
Memorial Şişli Hastanesi IVF Laboratuvarı olarak misyonumuz; etik ilkelerden ödün vermeden dünya standartlarında ve kanıtlanmış en ileri tekniklerini kullanarak, kalite kontrolünü sağlamak ve gerek ülkemiz gerekse yurt dışından başvuran hastalarımıza en üst kalitede ve güvenlikte hizmet sağlamaktır.
Yumurtalıklardaki olgun olmayan yumurtalar, hormonlar ile uyarılarak istenilen büyüklüğe geldiğinde, göbekten uygulanan yumurta çatlatma iğnesi (yumurtaların olgunlaşmasının tamamlaması için OPU işleminden önce mutlaka yapılması gereken bir iğne) yapıldıktan 35-36 saat sonra doktor tarafından ultrasonografi probuna ilave edilmiş bir OPU iğnesi eşliğinde yumurtalar steril bir tüp içerisine aspire (çekilerek) edilir ve embriyoloji laboratuarına gönderilir. Embriyoloji laboratuarında bir embriyolog tarafından steril tüp içerisinde gelen yumurtalar, mikroskop altında folikül (yumurta kesesi) sıvısı içinden steril tek kullanımlık cam pipet yardımıyla alınır. Gelişimini devam ettirebileceği başka bir kültür sıvısı içerisine konulur. İşlem yumurta sayısına bağlı olarak yaklaşık 15-20 dakika sürer.
Yumurta çatlatma iğnesinin mutlaka doğru zamanda ve doğru şekilde yapılması çok önemlidir. Çatlatma iğnesinin yanlış yapılması durumunda yumurtalar gelişimlerini tamamlayamazlar. Sonuç olarak, mikroenjeksiyon ya da IVF(tüp bebek) için yeterli olgunlukta ve sayıda yumurta elde edilemez. OPU, hastanın isteğine bağlı olarak genel veya lokal anestezi altında yapılmaktadır. Bu durumun önceden kararlaştırılması gereklidir. OPU, kolay ve genellikle ciddi ağrıya yol açmayan bir işlemdir. İşlem anestezi altında yapılacak ise işlem gününden önceki akşam saat 24:00'den itibaren hiçbir şey yiyip içmemeniz ve sabah size bildirilen saatte aç olarak merkezimize gelmeniz istenecektir. İstenilen saatte merkezimizde bulunmanız yumurtaların zamanında toplanma için dikkat edilmesi gereken konulardan biridir. Yumurtalar vaktinde toplanmadığı durumda ovulasyon (yumurtlama) gerçekleşir. Yumurtalarınız, yumurtalıklardan ayrılarak döllenme kanallarına gider. Bu kanallardan yumurtaları almak mümkün değildir. Bu nedenle yumurtalar mutlaka OPU saatinde toplanmalıdır.
Yumurta toplama işleminden sonra oluşabilecek olası kasık ağrısı için günde 2-3 tablet parasetamol(ağrı kesici) alınmasında sakınca yoktur. İşlem bittikten sonra bir süre sulu gıdalarla beslenme sağlanıp yaklaşık iki saat sonra hastanemizden ayrılmaya izin verilir. Bu süre içinde hemşireler tarafından hastanın kontrolleri yapıldıktan sonra taburcu edilerek yapılması gerekenler sözlü ve yazılı olarak bildirilir.
Yumurta toplama işleminden sonra cinsel ilişkide bulunulmamalıdır. İşlemden 24 saat sonra banyo yapılmasında bir sakınca yoktur. Evde istirahat edilmeli, 24 saat içinde araba kullanılmamalıdır.
38'den yüksek ateş.
Aşırı vajinal kanama (bir miktar kanama olması normaldir).
Çok şiddetli ve devam eden ağrı (bir miktar ağrı olması normaldir).
Ani kilo artışı.
İşlemden 8-10 saat sonrasında artan ağrı ile birlikte idrar miktarında azalma, idrarın koyulaşması veya idrar yapamama.
Bulantı, kusma, ishal, nefes almada zorluk, karında gerginlik.
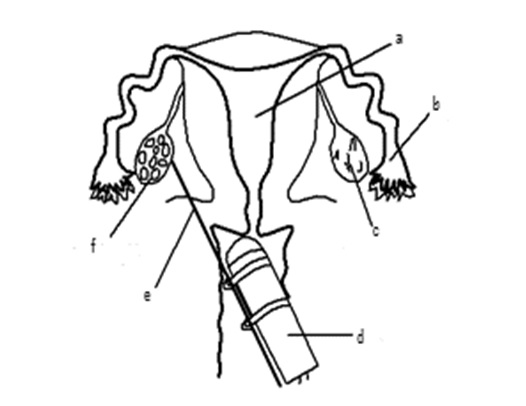
a: Uterus
b: Tuba uterina
c: Over
d: Ultrason probu
e: Aspirasyon iğnesi
f: Foliküller
Yumurta toplanması genellikle vajina içinden ultrasonografi
ile yönlendirilen bir iğne aracılığı ile yönlendirilir.
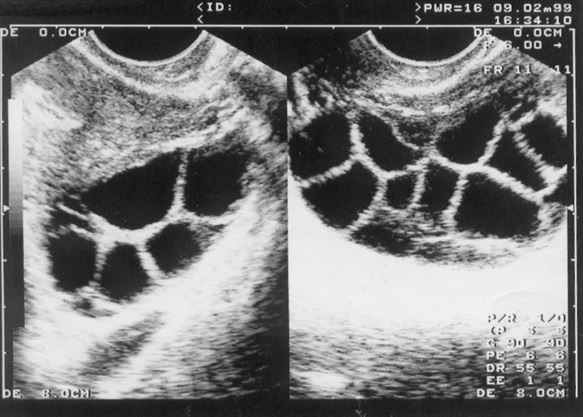
Ultrasonografi ile görüntülenen foliküller
Yumurtaların OPU sırasında değerlendirilmesi
OPU esnasında toplanan yumurtaların embriyolog tarafından yumurtayı çevreleyen kümülüs hücrelerine bakılarak Kümülüs-Oosit Kompleksi (COC) değerlendirmesi yapılır.
Tip I ve Tip II (Matür) COC;
Kümülüs hücreleri ışınsal radyal dağılım gösterir.
Kümülüs kompleksi gevşek yapıdadır.
Korona radiata hücreleri hafif-kompakt görünümlüdür.
Granüloza hücreleri genişlemiş ve düzenli kümeler şeklinde görülür.
Perivitellin aralıkta birinci polar body belirgindir.
Ooplazma net olarak gözlenir.
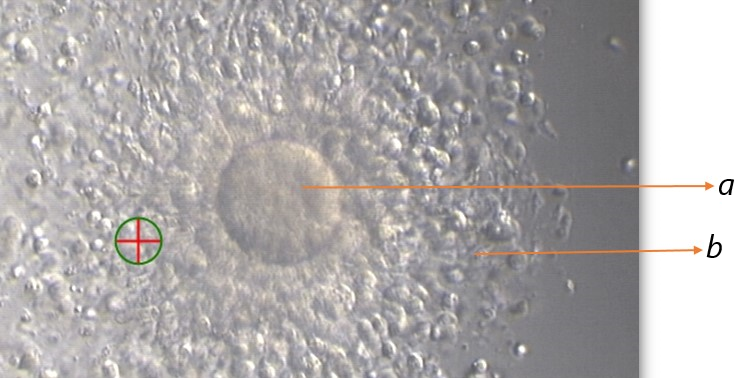
a: Ooplazma
b: Kümulus-korona hücreleri
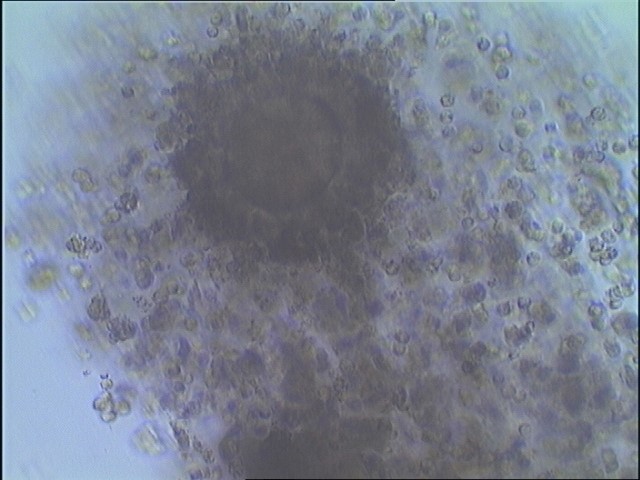
Tip III-Tip IV (İmmatür) COC;
Kümülüs ve korona radiata hücreleri yoğun dağılım gösterir.
Granuloza hücreleri koyu renkli ve kompakt yapıdadır.
Bazı vakalarda dejenere/atretik veya boş zona oosit (Yumurtanın dış zarına sahip, ooplazmasız oosit) alınabilir.
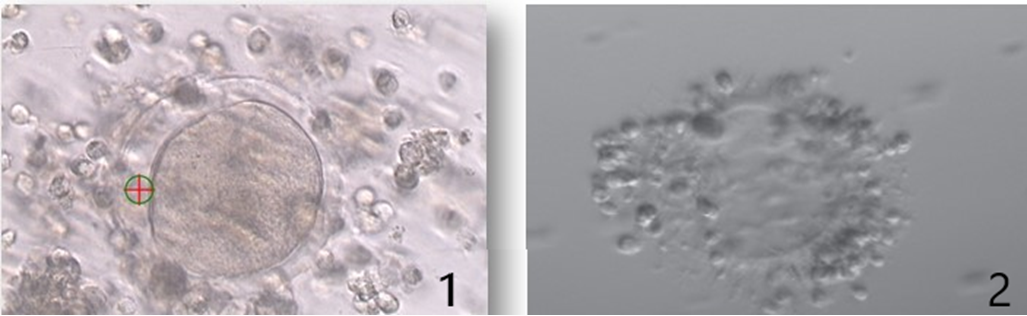
1 : Dejenere / atretik oosit 2 : Empty zona oosit
Mikroenjeksiyon Öncesi Yumurtaların Hazırlanması (Denüdasyon İşlemi)
Foliküllerden (yumurta kesesi) aspire edilen yumurtalar etrafındaki hücre kümesi ile birlikte alınır. Bu hücre kümesi yumurtaların olgunluğunu tamamlayabilmesini sağlar. Yaklaşık 2-3 saat bu hücreler yumurtanın etrafından uzaklaştırılmaz. Yumurtanın son olgunlaşma aşamasını tamamlaması beklenir. Bekleme süresinin sonunda hyaluranidaz adı verilen enzim ve steril cam pipetler yardımı ile yumurtanın çevresindeki hücreler enzimatik ve mekanik yöntem ile yumurtadan uzaklaştırılır. Böylece yumurtalar matürasyon (olgunluk) açısından değerlendirilebilecek duruma gelir. Denüdasyon işleminden yaklaşık 30-60 dakika sonra olgunluğunu tamamlamış yumurtalara mikroenjeksiyon işlemi uygulanır.
IVF(tüp bebek) (sperm ile yumurtanın aynı kültür sıvısı içine konularak spermin yumurtayı kendi kendine döllemesi işlemi) uygulanan yumurtalara denüdasyon işlemi mekanik yöntemle yumurtaların toplanmasından 22-24 saat sonra uygulanır.
|
|
|
|
Olgun olmayan (Profaz I) |
Olgun olmayan (Metafaz I) |
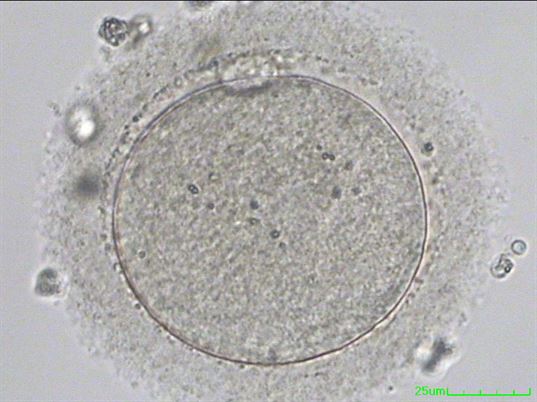
Olgun oosit (Metafaz II)
MİKROENJEKSİYON (İNTRASİTOPLAZMİK SPERM ENJEKSİYONU)
Mikroenjeksiyon, şiddetli erkek kısırlığı tedavisi için geliştirilmiş bir yardımcı üreme tekniği yöntemidir. Spermin normal dölleme özelliğine sahip olmaması durumunda spermin yumurta içine direkt olarak enjekte edilerek döllenme amaçlanır. Şiddetli erkek kısırlığına yol açan durumlarda IVF yöntemi de dahil olmak üzere bilinen diğer tedavi yöntemleri ile döllenme olmamakta veya çok düşük oranda gerçekleşmektedir. Sayı, hareketlilik ve şekil bozukluğu olan spermlerin kendiliğinden yumurtaları döllemesi mümkün olmamaktadır. Mikroenjeksiyon uygulaması, mikro-pipetler yardımı ile mikroskop altında spermin, kadından elde edilen yumurtanın içine enjekte edilmesidir. İşlemler mikroskobun ısıtılmış yüzeyinde, 200–400 kat büyütme altında ve mikromanipülatör aracılığı ile yapılmaktadır.

ICSI işlemi için kullanılan mikropipetler
Mikroenjeksiyon şiddetli erkek kısırlığı dışında, IVF (tüp bebek) ile döllenme sağlanamayan veya IVF(tüp bebek) için uygun sperm ve yumurta sayı ve/veya kalitesine sahip olmayan çiftlerde uygulanmaktadır. Menideki çok az sayıda spermle işlem yapılabildiği gibi menide spermin bulunmadığı durumlarda testislerden elde edilen spermler kullanılarak da mikroenjeksiyon yapılabilir. Bazı erkeklerde testislerde sperm bulunması mümkün olmayabilir. Bu durumda eğer varsa spermatid adı verilen ve spermin olgunlaşmamış halini oluşturan hücreler kullanılmaktadır. Spermatid kullanımı ile elde edilen sonuçlar henüz başarılı değildir. Düşük oranda döllenme ve gebelik elde edilebilmektedir. Ülkemizde ilk spermatid uygulamaları tarafımızdan başlatılmış olup “dünya tıp literatüründe” yer alan ilk spermatid ikiz gebeliği tarafımızdan elde edilmiştir. Mikroenjeksiyon yöntemi son yıllarda kısırlık tedavisinde devrim yaratmış olup daha önceden tedavi şansı verilmeyen birçok çift bu yöntemle çocuk sahibi olmuştur. Prof. Dr. Semra Kahraman ve ekibi, 1994 yılında ülkemizde ilk kez mikroenjeksiyon uygulamasını gerçekleştirmiş ve bu konuda önderlik yapmışlardır. Başlangıçta menideki spermler ile mikroenjeksiyon yapılmış, ardından epididim ve testis spermleri kullanılarak ilk uygulamalar gerçekleştirilmiştir. ICSI, TESA, MESA, TESE, PESA ve mikro-TESE uygulamaları ile Türkiye'de ilk canlı doğumla sonlanan gebelikler elde edilmiştir. Mikroenjeksiyon işlemi özel donanıma sahip mikroskop altında, uçlarına açı verilmiş steril tek kullanımlık cam mikropipetler ile gerçekleştirilir.
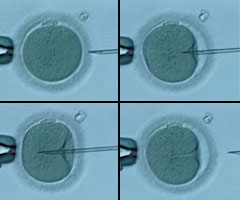
Intrasitoplazmik sperm enjeksiyonu
Yumurta toplama işlemi sonucunda elde edilen yumurtalar önce çevresindeki kümülüs (hücre kümesi) hücrelerinden temizlenerek olgun olanlar ve kullanılabilecek durumdakiler belirlenir. Mikroenjeksiyon işlemi yapılacak olan steril, toksik olmayan plastik kapta, önce erkeğe ait spermlerin konulacağı özel kültür sıvısı içeren bir havuz oluşturulur. Daha sonra olgun yumurtaların konulacağı özel besi sıvısı içeren mikro damlacıklar hazırlanır. Sperm ve yumurta kendilerine ait yerlere konulduktan sonra mikroskop altında şekil olarak normal görünümlü ve varsa hareketli sperm seçilerek mikroenjeksiyon pipeti ile kuyruğun orta bölümüne bastırılarak hareketsizleştirilir. Kuyruk kısmından yakalanan sperm pipet içine alınarak yumurtanın içinde olduğu damlaya gidilir. Özel tutma pipeti ile sabitlenen yumurtanın içine hareketsizleştirilen sperm enjekte edilir(konulur). Bu işlem tüm yumurtalara aynı sıra ile uygulanır. İşlem bittikten sonra yumurtalar özel besi ortamlarına alınarak işlemden 18 – 20 saat sonra döllenme kontrolü yapılır. Şiddetli erkek kısırlığında spermler yumurtayı dölleme yeteneğinden yoksundur. Şiddetli erkek kısırlığı için standart bir tanım yoktur ancak ileri hızlı hareketli ve normal morfolojideki sperm sayısının bir milyon altında olması şeklinde tanımlanabilir. Sperm ve yumurtanın tamamen normal olduğu durumlarda bile tüp bebek yöntemi ile döllenme olmayabilir. IVF yöntemi ile döllenmenin olmadığı durumlarda mikroenjeksiyon işlemine geçilmektedir. İzah edilemeyen kısırlık durumunda IVF yöntemi ile % 15–20 oranında döllenme oluşmamaktadır. Bu çiftlerde sperm parametrelerinin normal olduğu düşünülerek doğrudan IVF yöntemi yapılır ise döllenme olmama ihtimali söz konusu olacağından yumurta sayısı yeterli olan çiftlerde (10 ve üzeri) mikroenjeksiyon ve IVF yöntemi birlikte yapılmaktadır. Böylece yumurtalar iki gruba bölünerek IVF yöntemi ile döllenme olup olmadığı kontrol edildiği gibi mikroenjeksiyon ile döllenmeme durumuna karşı önlem alınır. Mikroenjeksiyon işlemi için çiftlerde bazı hazırlıkların yapılması gereklidir. Erkekte değerlendirme yapılırken 3-4 hafta ara ile en az 2 kez meni örneği alınır ve mikroenjeksiyon işlemi için aday olup olmadığı araştırılır. Her değerlendirme için ortalama 3–5 günlük cinsel perhiz gereklidir. Erkeklerde ürolojik inceleme yapılır. İlave tetkikler, operasyon veya ilaç tedavisine gerek olup olmadığı araştırılır. Kadında ise üreme organlarının yapısı ve yumurtalıkların tedaviye vereceği cevabın araştırılması için yardımcı testler uygulanır.
Günümüzde erkek kısırlığında ICSI ile böylesine umutlu bir tedavi olanağı sağlanmasına rağmen başarıyı belirleyen en önemli faktörler kadının yaşı ve elde edilen yumurtaların kalitesidir. İlerlemiş kadın yaşı ve buna bağlı artmış kromozom anomalileri nedeni ile erkek kısırlığı tedavisinde başarı halen kadına ait faktörlere bağlı olarak değişmektedir. 35 yaş ve üzeri kadınların yumurtalarındaki kromozom anomalisi oranı artmakta, bu durum verilen embriyoların implante olmasını (rahim duvarına tutunma) ya da oluşmuş ise gebeliğin düşükle sonlanması riskini artırmaktadır. Bazı kadınlarda ise yaşa bağlı olmaksızın azalmış yumurtalık kapasitesi nedeni ile az sayıda ve kötü kalitede elde edilen yumurtalarda döllenme sorun olmakta ve kötü embriyo kalitesi elde edilmektedir. Normal gebeliklerde olduğu gibi yardımcı üreme teknikleri ile elde edilen gebeliklerde de düşük riski mevcuttur. Özellikle 40 yaş ve üzerindeki kadınlarda gebelik oranları ciddi olarak azalmaktadır. Yumurtalık fonksiyonları normal veya sınırda bozuk bulunan 40 yaş üstü kadınlarda tüp bebek işlemleri düşük başarı oranları çiftlere bildirilerek uygulanmaktadır.
Merkezimiz, günümüze kadar tüp bebek tedavileri ile ilgili edindiği bilgi birikimi ve deneyimleri nedeniyle Sağlık Bakanlığı tarafından Eğitim Merkezi olarak kabul edilmiştir. Yurtiçi ve yurtdışı katılım ile bugüne kadar 200’ün üzerinde doktor, embriyolog, biyolog, teknisyen ve hemşire eğitim almıştır. Merkezimizde ayda ortalama 230-270 çifte mikroenjeksiyon ve tüp bebek uygulaması yapılmaktadır.
IMSI (Yüksek Mikroskobik Büyütmeyle Seçilmiş Sperm Mikroenjeksiyonu)
Yardımcı Üreme Teknikleri alanındaki en son gelişmelerden birisi olan IMSI (Intracytoplasmic Morphologically Selected Sperm Injection-Yüksek mikroskobik büyütme ile normal yapıda olduğu saptanan spermin mikroenjeksiyonu) uygulaması, gerekli teknik altyapının tamamlanmasının ardından Mayıs 2008’den itibaren merkezimizde uygulanmaktadır.
Mikroenjeksiyon işlemi (ICSI), 200–400 kat mikroskobik büyütme altında hareketli spermler arasından şekil olarak en düzgün olanların seçilmesine imkan vermektedir. Fakat bu durum spermin döllenme, embriyo gelişimi ve gebelik için çok önemli olan bozuklukların tanımlanmasına imkan vermemektedir. Androloji laboratuvarında özel boyama teknikleri ile bu bozukluklar tanımlanabilmekte fakat bu spermler boyama sonrası canlı kalamadıklarından mikroenjeksiyon için kullanılamamaktadır. IMSI işleminde kullanılan yüksek büyütmeli objektifler ve özel optik sistemler aracılığı ile mikroenjeksiyon için hazırlanan spermleri 8050 kata kadar büyütmek ve spermin başı içerisindeki bozuk yapıları ayırt ederek seçim yapmak mümkün olmaktadır.
Özellikle 2005 yılından bu yana yoğun olarak yapılan çalışmalarda; sperm başı içerisindeki genetik materyali içeren çekirdek kısmında bulunan vakuoller (sıvı dolu kesecikler), DNA yapısında hasar bulunabileceği konusunda ipucu vermektedir. Sperm DNA yapısındaki hasarlar, döllenme başarısızlığı, embriyo gelişiminin durması, kötü ve/veya yavaş embriyo gelişimi gibi problemlere sebep olabilmekte ve dolayısıyla gebelik şansını olumsuz etkilemektedir.
Şiddetli erkek faktörü olan vakalarda, tekrarlayan tüp bebek başarısızlığında ve nedeni izah edilemeyen kısırlık durumlarında spermin rolünü anlamaya ve uygun yapıdaki spermlerin seçilmesine olanak veren IMSI sistemi, blastosist evresine ulaşabilecek iyi embriyoların gelişimine de imkan vermesi yönünden bu alandaki yeni ve önemli gelişmelerden biridir.
IMSI
|
|
|
|
Klasik ICSI'de görülen sperm |
IMSI işleminde görülen sperm -8050 büyütme- Baş anomalileri kolaylıkla seçilebilmekte |
|
|
|
|
IMSI-8050 büyütme- |
IMSI-8050 büyütme- |
|
|
|
|
8050 büyütme |
8050 büyütme |
DÖLLENME ORANI DÜŞÜK OLGULARDA YAPAY OOSİT AKTİVASYONU
Tüp bebek tedavisinde mikroenjeksiyon (ICSI) işlemi sonrasında vakaların %2 ila 3’ünde döllenme başarısızlığı olmaktadır. Sitolojik incelemeler, bu durumun %50 den fazlasının oosit (yumurta) aktivasyonunun yetersizliğinden olduğunu ortaya koymuştur. Döllenme (fertilizasyon) başarısızlığı oosit ve/veya sperme ait farklı nedenlerle olabilir. Oositlerin sitoplazma kısmında olgunlaşma olmaması ve genetik nedenler fertilizasyon başarısızlığının ana nedenleridir. Sperme bağlı nedenler ise; canlı sperm olmaması, kromozomal nedenler, sperm nükleusunda kondensasyon bozuklukları ve sperm organel eksikliği nedeniyle fertilizasyon olamayabilir.
Merkezimizde önceki denemelerinde düşük fertilizasyon öyküsü ya da fertilizasyon başarısızlığı olan; sperm baş morfolojisinde ciddi morfolojik anomali (globozospermi, makrosefali) olan veya sperm konsantrasyon (sayı), motilite (hareket) ve vitalite (canlılık) problemi olan vakalarda ve dondurulmuş testis spermi kullanılacak vakalarda, Mikro TESE sonrası az sayıda sperm elde edilen ya da sonrası matür (olgun) sperm elde edilemeyen vakalarda spermatidlerin (spermin olgun olmayan öncü hücresi) kullanılması gereken durumlarda fertilizasyon oranını arttırmak için oosit aktivasyonu yapılmaktadır.
Oosit aktivasyonu
1. Mekanik
2. Kimyasal
3. Elektriksel aktivasyon olmak üzere 3 farklı yolla uygulanabilir.
Mekanik Aktivasyon: Mikroenjeksiyon işlemi sırasında oosit sitoplazmasının ICSI pipeti içine daha fazla aspire edilmesi ve yumurta içinde hücre zarına yakın bölgeye bırakılması ile olur. Etkinliği diğer aktivasyon metodlarına göre daha düşüktür.
Kimyasal Aktivasyon: Fertilizasyon sperm hücresinin yumurta içerisine girdikten sonra tetiklediği bir dizi reaksiyon ile başlar. Öncelikle spermin baş kısmında yer alan oosit aktive edici faktör (SOAF), fosfolipaz c zeta proteinini kullanarak fertilizasyonu başlatır. Fertilizasyonda hücre içi kalsiyum (Ca++) artarak ICSI’den 30 dk sonra pik yapar, 4-5 dakika sonrasında ise azalır. Kalsiyum düzeylerindeki bu dalgalanmalar her 30 dk da 1 kez olmak üzere 3-4 saat devam eder. Sperm ya da oositte bulunan bu protein ya da enzimlerin yetersizliği ya da yokluğu fertilizasyon başarısızlığı ile sonuçlanabilir.
Özetle yumurtaya ait problemler nedeni ile hücre içinde yetersiz Ca++ varlığı ya da sperm başında mevcut olan oosit akivatörlerinin yetersizliği nedeniyle yumurta içerisinde yetersiz Ca++ salınımı, döllenmenin olmamasına yol açabilir. Bu durumda hücre dışından Ca++ iyonlarının hücre içine geçişini sağlayan veya hücre içinde depolanmış Ca++ iyonlarının boşaltılmasını uyaran kimyasal maddeler ve özel antibiyotikler kullanılır. Bu kimyasallar çok çeşitli olmakla birlikte en sık kullanılanları Iyonomisin, Strosiyum Klorür (SrCl2) ve Kalsimisin (A23187) dir. Merkezimizde de yukarıda belirtilen endikasyonlarda etkinliği diğerlerine göre daha fazla olduğu çalışmalarla desteklenen Iyonomisin kullanılmaktadır.
Elektriksel Aktivasyon: Elektriksel oosit aktivasyonu yönteminde, işlem uygulanacak yumurta hücreleri, mikroenjeksiyon işleminden 30 dk sonra özel kültür kapları içine konumlanmış elektrotların arasında bulunan özel iletken tampon sıvıları içine konur ve çok düşük düzeylerde (mikrovolt) akım verilerek oositin ve spermin polarize olması sağlanır. Böylece hücre içi Ca++ artışı sağlanarak fertilizasyon mekanizmalarının tetiklenmesi amaçlanır.
Elektriksel aktivasyon özellikle kimyasal aktivasyonda sonuç alınamayan durumlarda ve mikroenjeksiyon için olgun spermi olmayan, sperm öncü hücreleri (Round spermatid, elonge spermatid) kullanılacak vakalarda uygulanmaktadır.

Elektriksel aktivasyon cihazı
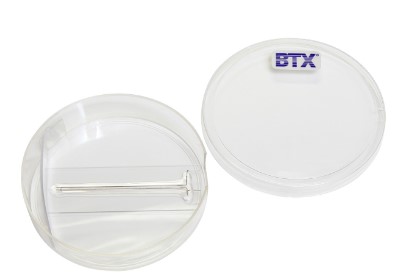
Paralel elektrotlu elektriksel aktivasyon kabı

Elektriksel aktivasyonda, mikroskop altında özel aktivasyon kabının paralel elektrotlarının arasına iletken sıvılar konur ve oositler bu sıvının içerisinde mikrovolt düzeyinde akıma maruz bırakılarak aktivasyon sağlanır
IVF (TÜP BEBEK) (In Vitro Fertilizasyon)
IVF ilk olarak 1978 yılında İngiltere’de uygulanmaya başlanmıştır. Bu yolla doğan ilk bebek olan Louise Brown, birçok çift için umut kaynağı olmuştur. Normal şartlarda bir kadın yumurtlama zamanında 1 veya 2 yumurta geliştirmesine karşın, IVF gibi yardımcı üreme tekniklerine ihtiyaç duyulduğu durumlarda, döllenen yumurta sayısı ve gelişen embriyo sayısının arttırılması amacı ile yumurtalıklar ilaçlarla uyarılarak yumurta sayısı arttırılır. IVF tekniği, mikroenjeksiyondan farklı olarak yumurtaların toplanmasından sonra yumurtalara denudasyon işlemi uygulanmadan gerçekleştirilir. IVF işleminde, hastanın eşinden alınan ve uygun yıkama yöntemleriyle en iyi spermlerin elde edildiği sperm örneği ve yumurtalar aynı ortamda bir araya getirilir. Spermin, yumurtanın içine kendi kendisine girmesi amaçlanır. Hastanın yaşı, yumurta sayısı, kalitesi, endikasyonu(kısırlık nedeni), sperm kalitesi (sayı, hareket, morfoloji), daha önce IUI(aşılama) ya da ART(tüp bebek) denemesinin olup olmadığı, sekonder kısırlık (daha önce gebe kalan fakat daha sonra kısır olan), PGT(Preimplantasyon Genetik Tanı) endikasyonu olup olmadığı değerlendirilir.
IVF (tüp bebek) Hangi Hastalara Uygulanabilir?
Her iki tüpü tıkalı ya da ameliyat ile alınmış olan hastalarda
Polikistik Over Sendromu (yumurtlama problemi) olan hastalarda
Hafif endometriosis, sperm değerleri normalin biraz altında olan hastalarda
Daha önce çocuk sahibi olmuş ve eşinin spermlerinde problem olmayan hastalarda
Daha önce IVF denenmiş ve başarılı sonuç alınmış hastalarda
Açıklanamayan kısırlık durumunda tüp bebek uygulaması ile % 70-80 oranında döllenme başarısı elde edilebilir. Bu çiftlerde sperm parametrelerinin normal olduğu düşünülerek doğrudan IVF (tüp bebek) uygulaması yapılır ise döllenme olmama ihtimali söz konusu olacağından yumurta sayısı yeterli olan çiftlerde (10 ve üzeri) mikroenjeksiyon ve IVF(tüp bebek) uygulaması birlikte yapılmaktadır. Böylece yumurtalar iki gruba bölünerek IVF(tüp bebek) uygulaması ile döllenme olup olmadığı kontrol edildiği gibi mikroenjeksiyon ile döllenmeme durumuna karşı önlem alınır.
ERKEN VE İLERİ DÖNEM EMBRİYO GELİŞİMİ
Tüp bebek tedavisinde en önemli basamak, laboratuvar şartlarında embriyo gelişiminin sağlanmasıdır. Döllenme sağlandıktan sonra laboratuvar koşulları ve çalışan ekibin tecrübesi dahilinde embriyo gelişimi takip edilerek uygun olan günde transfer işlemi gerçekleştirilir.
Ancak transfer günleri merkezlerin stratejilerine, çiftin elde edilen yumurta sayısına, gelişmekte olan embriyo kalitesine göre değişim göstermektedir. Memorial Hastanesi Tüp Bebek Merkezi‘nde, döllenmeden sonra embriyo gelişiminin 2, 3, 4, 5 ve 6. günlerinde embriyo transfer işlemi yapılabilmekle birlikte uygun şartlarda blastosist gelişiminin gerçekleştiği 4., 5. ve 6. gün transfer uygulaması tercih edilmektedir.
Erken Embriyo Gelişimi
Pronüklear değerlendirme ve sınıflandırma
Döllenme kontrolü IVF veya mikroenjeksiyon işleminden 16-20 saat sonra yapılır. Döllenme, kısaca tek bir sperm çekirdeğinin oositten gelen çekirdek ile aktive olmuş oosit sitoplazması içinde birleşmesi olarak özetlenebilir. Normal fertilizasyonda 2 pronükleus ile birlikte birinci ve ikinci kutup cisimciği gözlenir.
Bu evrede değerlendirilen parametreler:
Pronükleusların (PN) pozisyonu ve boyutu,
Çekirdekçik öncül cisimciklerinin (NPB) sayısı, büyüklüğü ve dağılımı,
Kutup cisimciklerinin yerleşimi ve sitoplazmik halonunu varlığı dikkate alınarak yapılır.
Yapılan çalışmalar PN oluşumu sırasında meydana gelen hatalar ya da asenkronizasyonun, embriyonun kromozal yapısı ve anöploidi ile ilişkili olduğu gösterilmiştir (Kahraman ve ark 2002).
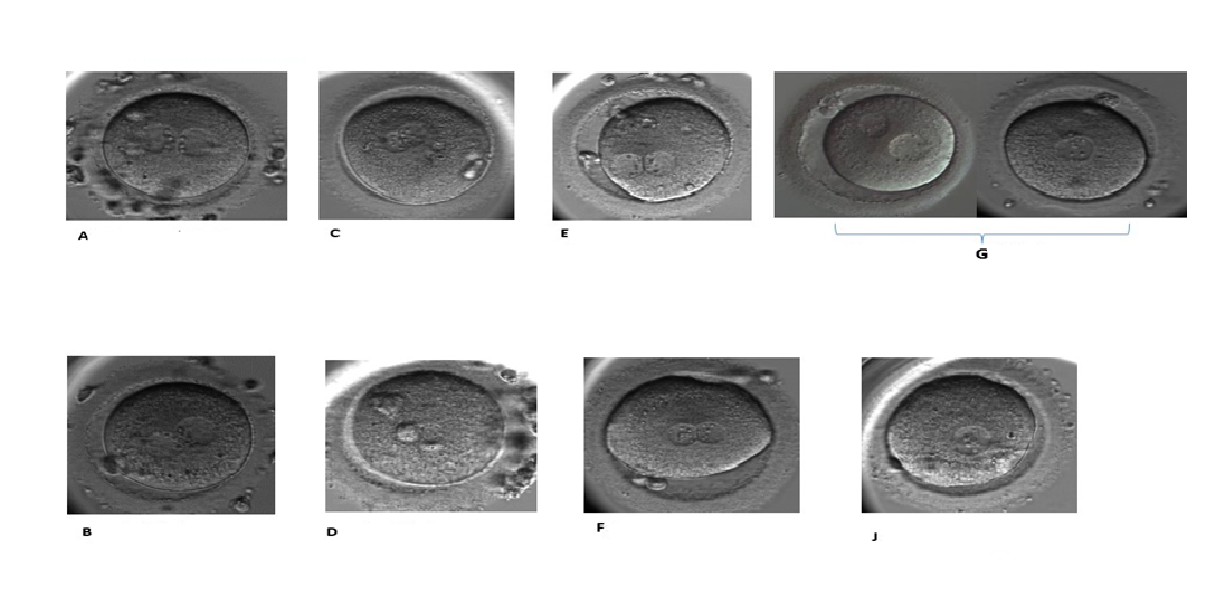
Merkezimizde pronükleus değerlendirmesi şu şekilde yapılmaktadır:
A: Çekirdekçik öncü cisimcikleri büyük, kesişim noktasında ve sıralı
B: Çekirdekçik öncü cisimcikleri küçük, kesişim noktasında ve sıralı
C: Çekirdekçik öncü cisimcikleri büyük ve dağınık
D: Çekirdekçik öncü cisimcikleri küçük ve dağınık
E: Çekirdekçik öncü cisimcikleri büyüklü küçüklü, kesişim noktasında
F: Çekirdekçik öncü cisimcikleri büyüklü küçüklü ve dağınık
G: Pronükleuslar birbirinden ayrı veya boyutları farklı
J: Erken singami(erken birleşme)
|
|
|
A,B,C,D,E,F normal döllenen zigot olarak kabul edilir ve embriyo gelişiminde fark gözlenmez. G,J olarak sınıflanan zigotlarda normal döllenen zigot olarak kabul edilir fakat diğerlerinden ayrı olarak takip edilir(Kahraman ve ark 2002).
Bölünme Evresi Sınıflaması
Döllenen bir yumurta yaklaşık 20 saat sonra ilk mitotik bölünmeye başlayarak 2 hücreli bir embriyo oluşturmaktadır. Bu dönemden itibaren embriyoların değerlendirmesi;
Blastomerlerin şekli ve boyutu,
Blastomerler arası fragmantasyon derecesi,
Blastomerlerdeki nukleus sayısı(multinükleasyon),
Sitoplazmik görünüm,
Erken kompaktlaşma gibi parametreler dikkate alınarak yapılır.
Bölünme hızına göre embriyonun sahip olduğu blastomer sayısı günün beklenen limitleri arasında ise normal gelişen bir embriyo, eğer bu sayı düşükse yavaş gelişen bir embriyo olarak değerlendirilir. Klivaj dönemi olarak adlandırılan ve embriyo gelişiminin 2.,3. ve 4. gününü kapsayan değerlendirmede 2. gün ve 3. gün sınıflaması Veeck ve arkadaşlarının oluşturduğu sınıflamaya dayanmaktadır. 4. gün sınıflaması ise Feil ve arkadaşlarının 2009 yılında oluşturduğu Morula sınıflamasını esas almıştır. Buna göre normal bölünme hızına sahip bir embriyo 22-25. saatte 2 hücre, 2.günde (42-44 saat) 3-4 hücre, 3.günde(66-68 saatte) 6-8 hücre ve 4.günde ise birleşme işaretlerine bağlı olarak 10 ve üzerinde hücreye sahip olan embriyodur. Kalite değerlendirmesine göre ise eşit büyüklükte blastomer yapısına sahip olan, % 0-5 arasında fragmantasyon içeren ve sitoplazmasında belirgin granüler yapı gözlenmeyen embriyolar "1. Kalite" olarak değerlendirilir. Bu değerlendirmeye göre kalite sıralaması şu şekilde olmaktadır;
|
1. Kalite |
Eşit blastomer büyüklüğüne sahip, %0-5 oranında fragmantasyon içeren ve |
|
2. Kalite |
Eşit blastomer büyüklüğüne sahip, %5-10 oranında fragmantasyon içeren veya |
|
3. kalite |
Blastomerler birbirinden hafifçe farklı, %10 üzerinde fragmantasyona sahip veya |
|
4. Kalite |
Blastomer sayısı net sayılamayan, %30 dan fazla fragmantasyona sahip, blastomerler birbirinden |
Embriyo kalitesinin düşüşüyle birlikte embriyonun ileri gelişim gösterme, canlılığını devam ettirme ve implantasyon potansiyeli de azalmaktadır.
|
|
|
|
|
44. saat 4 hücreli |
72. saat 8 hücreli ve |
72. saat 8 hücreli ve |
İleri Dönem Embriyo Gelişimi
Bu dönemde yapılan embriyo sınıflaması Feil ve arkadaşlarının 2008 yılında oluşturduğu sınıflama ile değerlendirilmektedir. Fertilizasyondan sonraki 4. günde gelişen embriyodaki hücre sayısı inseminasyonu takiben yaklaşık 96 saat sonra 16–20 hücre arasındadır. Kompaktlaşma hücrelerin daha yakın bir şekilde yapışmasına neden olan bir seri hücreler arası sıkı bağlantıların (dezmozom, gap junction) oluşması sonucu meydana gelir. Embriyo kompaktlaşmaya başladığı zaman morula adını alır. Moruladan sonra kavitasyon dönemi başlar. Kavitasyonun oluşması ile kaviteden salgılanan sıvı, blastosöl oluşumunu tetikler. Kavitasyon ilerledikçe kompaktlaşma sırasında hücrelerin (blastomerlerin) kutuplaşmasıyla iki farklı hüre grubunu (trofoektoderm-dış hücre kütlesi ve inner cell mass-iç hücre kütlesi) oluşturacaktır.
4. gün embriyolarının kalite değerlendirmesi şu şekilde yapılmaktadır;
|
1. Kalite |
Early blastosist,kavitasyon ve full morula ve herhangi bir anomali |
|
2. Kalite |
Morula veya compact embriyo morfolojisine sahip en az bir anomalinin |
|
3. kalite |
Morula veya compact embriyo morfolojisine sahip 2 veya 3 anomalinin eşlik ettiği veya |
|
4. Kalite |
Blastomer sayısı 10 veya daha az sayıda olan herhangi bir birleşme bulgusu |
|
|
|
|
|
4. gün 10 hücreli birleşme başlangıcı |
96. saat 4.gün morula aşamasındaki 2. kalite embriyo |
96. saat 4. günde kavitasyon izlenen |
Blastosist oluşumu inseminasyondan sonra 5. ve 6. günlerde gerçekleşir.
Embriyoları blastosist dönemine kadar takip etmenin önemli avantajlarından birisi de yavaş gelişen veya gelişimi duraksamış embriyoların ayırt edilebilmesidir.
Blastosist gelişiminin gözlenmesi ve blastosist transferinin yapılması, embriyonun rahim içine tutunmasını ve dolayısı ile asıl hedef olan gebelik şansının artmasını sağlar. Merkezimizde blastosist aşamasındaki embriyo transferi ile sağlanan gebelik oranları %65–70 dolaylarındadır.
Bilindiği gibi son yıllarda tüp bebek tekniklerinin kullanımına bağlı olarak çoğul gebelikler daha sık görülmektedir. Bunun en önemli nedeni fazla sayıda embriyonun rahime transfer edilmesidir. Blastosist transferi ile daha yüksek oranda gebelik elde etmek amaçlandığı gibi düşük sayıda ve en iyi kalitede seçilmiş olan 1 veya 2 embriyonun transferi ile çoğul gebeliklerin neden olabileceği riskler azaltılmaktadır. Merkezimizde bir veya iki blastosist transferi yapılan vakalarda üçüz gebelik görülme oranı %1’in altındadır
Merkezimiz bu stratejiyi başarı ile 5 yıldır sürdürmekte olup, çoğul gebelik oranlarında dramatik azalmalar sağlanmakla birlikte yüksek gebelik oranları elde edilmektedir. Aynı zamanda embriyo transferi sonrası blastosist seviyesindeki embriyolar vitrifikasyon yöntemi ile başarılı bir şekilde dondurularak saklanmaktadır.
Blastosist aşamasında farklılaşmış iki tip hücre mevcuttur. Bu iki farklı hücre grubundan en önemlisi iç hücre kitlesi olarak tanımlanan ve gebelik esnasında embriyoyu oluşturmakla görevli olan hücre kitlesidir. Diğeri ise dış hücre kitlesi (trofoblast) olarak tanımlanan ve gebelik esnasında gebelik kesesi ve bebeğin beslenmesi için gerekli kısımları oluşturan hücre kitlesidir.
Blastosist skorlama sisteminde her bir embriyoya aşağıdaki kriterlere göre 3 ayrı skor verilir,
Blastosist gelişim seviyesi (kavitasyonun başlangıcından tomurcuklanmaya kadar)
İç hücre kütlesi kalitesi
Dış hücre kütlesi kalitesi
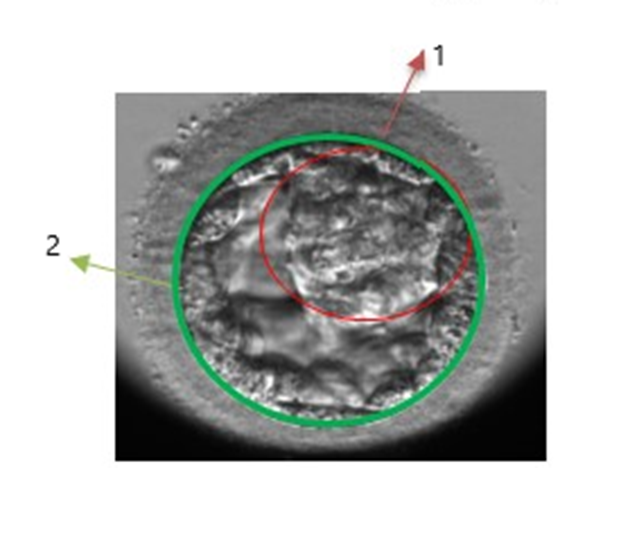
1: İç hücre kitlesi
2: Dış hücre kitlesi
|
Skor |
Blastosist Ekspansiyonuna Göre Değerlendirme |
|
1 |
Kavitasyonun başlaması, blastosöl hacminin embriyo hacminin yarısından az olması |
|
2 |
Blastosöl hacminin embriyo hacminin yarısından fazla olması |
|
3 |
Blastosöl hacminin embriyo hacminin tamamını kaplaması |
|
4 |
Blastosöl hacminin embriyo hacminden büyük olması, dış çeperin incelmesi |
|
5 |
Dış çeperin kırılarak tomurcuklanmanın başlaması |
|
6 |
Embriyonun dış çeperden tamamen ayrılması, tomurcuklanmanın tamamlanması |
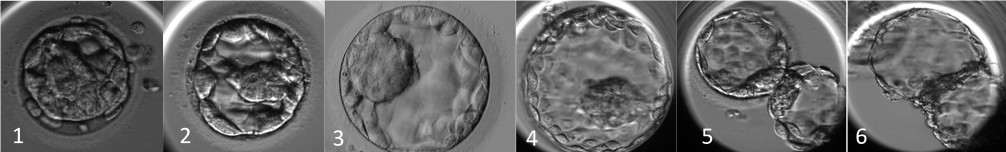
Ekspansiyon Seviyesine Göre Blastosist Kalitesi
|
Skor |
İç hücre kitlesi kalitesi |
|
A |
Sıkı paket halinde çok hücre içermesi |
|
B |
Gevşek ama birçok hücre içermesi |
|
C |
Çok az sayıda hücre içermesi |
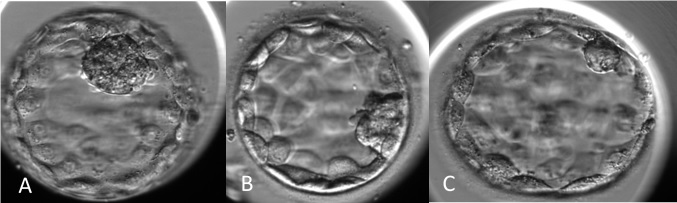
İç Hücre Kitlesine Göre Blastosist Kalitesi
|
Skor |
Dış hücre kitlesi kalitesi |
|
A |
Birbirine sıkıca bağlı birçok hücreden oluşan epitel yapı |
|
B |
Daha gevşek bağlı birkaç hücreden oluşan epitel yapı |
|
C |
Çok az ve büyük hücrelerden oluşan epitel yapı |
Dış Hücre Kitlesine Göre Blastosist Kalitesi
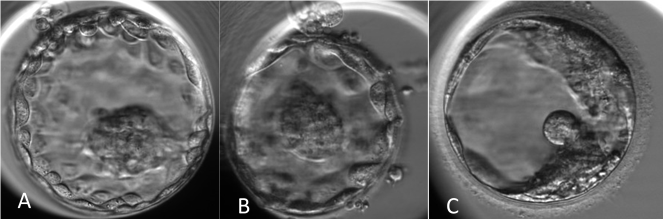
Hepatit ve HIV Taşıyıcı Vakalarda Laboratuvar Çalışma Algoritması
Tüp Bebek kliniğimize başvuran hastalardan, serolojik kan örnekleri alınarak tedavi öncesinde HIV, Hepatit B ve Hepatit C virüsü taşıyıcılıkları araştırılır. Taşıyıcılığı olan çiftlerde uluslararası bilim kurulunun önerisi kontaminasyon (bulaş) riskini azaltmak için viral yüklü vaka örneklerinin çalışma alanının diğer vakalardan farklı alanlarda yapılması yönündedir. Dondurulmuş sperm, oosit(yumurta), embriyo, testis dokusu gibi örneklerde sıvı nitrojende(-196C) dahi HIV, HCV, HBV gibi virüslerin yaşayabileceği ve nitrojen tanklarında örneklerin çapraz kontaminasyona neden olabileceği düşünülmektedir. Dondurulmuş viral yükü negatif örneklerin korunması için HIV, HBV ve HCV yüklü vakaların ayrı tanklarda saklanması önerilir.
Viral yüke sahip erkek hastaların semen örnekleri beyaz kan hücrelerinin ve seminal sıvıdaki serbest virüs seviyesinin azaltılması için 3 tabakalı gradient yöntemi kullanılarak hazırlanır. Bu yöntemde farklı konsantrasyona sahip gradient mediumu ile tabakalar oluşturulup spermin tabakalardan geçerek seminal plazmadan ayrılması sağlanır. Ayrıca semen örnekleri gradient ile yıkama işlemi sonrasında az bir kısmı eleminasyonun başarılı olup olmadığını test etmek amacı ile biyokimya laboratuvarına gönderilirken, diğer kısmı ise dondurulur. Test sonucu temiz ise, dondurulmuş örnek mikroenjeksiyon işlemi yapılacağı gün çözülür ve kullanılır.
Merkezimizde viral yüklü vakaların işlemleri (yumurta toplama, sperm hazırlama, gamet ve embriyo dondurma) diğer vakalardan ayrı, farklı çalışma ortamlarında yapılmaktadır. Oosit ve embriyo kültürü için karantina inkübatörleri kullanılmakta ayrıca viral yüklü vakaların dondurulan tüm gamet(sperm/oosit) ve embriyoları yüksek korumalı taşıyıcılar ile dondurularak diğer vakaların örneklerinden ayrı, viral yükün çeşidine göre farklı karantina tanklarında saklanmaktadır.
Embriyoskop (TLI) : Tüp Bebek Tedavisinde Sürekli Embriyo İzleme Sistemi
Natürel siklusta ovülasyon sonrası yumurtanın sperm tarafından döllenmesi ve embriyoya dönüşmesi tüplerde gerçekleşmektedir. Embriyo, döllenme sonrası rahim duvarına tutunmasına kadar geçen süre zarfında tüp ve rahim tarafından kendisine sağlanan en uygun besin, sabit pH ve sıcaklık ortamında gelişimini sürdürmektedir.
Tüp bebek teknikleri ile en yüksek gebelik şansını sağlayabilmek için yumurta toplanmasından embriyonun rahim içine transferine kadar geçen sürede embriyonun gelişimi için gereken en uygun koşulları laboratuvarda sağlamayı amaçlamaktadır.
Embriyonun gelişimi için ihtiyaç duyduğu ısı, embriyoyu dış etkenlerden koruyan inkübatörler aracılığı ile sağlanmaktadır. Embriyonun ihtiyaçları içine yerleştirildiği kültür ortamı ile karşılanmaktadır. En uygun pH değerleri ise gerek inkübatör içerisinde belirli bir düzeyde tutulan karbondioksit gazı ile gerekse kültür ortamındaki maddeler ile sabitlenmektedir.
Laboratuvar ortamında döllenmenin ve gelişimin değerlendirilebilmesi ve rahim duvarına tutunma olasılığı en yüksek olan embriyonun belirlenebilmesi için belirli aralıklarla (1., 3., 4. ve 5. günlerde) inkübatörden kısa süreliğine (maksimum 1-2 dakika) çıkarılıp mikroskop altında incelenmesi gerekmektedir.
Sıcaklık, pH değişimlerine ve dış etkenlere son derece hassas olan embriyonun inkübatör dışında kaldığı süreyi en aza indirgemek için uzun zamandır devam eden çalışmaların sonucunda Sürekli Embriyo İzleme Sistemi (TLI) geliştirilmiştir. Sürekli Embriyo İzleme Sisteminin ana amacı her bir embriyonun gelişiminin inkübator içerisinde bu cihaz için özel olarak geliştirilen bir kamera sistemi ile devamlı olarak kayıt altına alınmasıdır. Sürekli Embriyo İzleme Sistemi ile kısa zaman dilimlerinde (20 dakika) gelişmekte olan embriyoya ait görüntüler alınmaktadır. Bu işlem sırasında kültür ortamının sıcaklık ve pH değerlerinde herhangi bir değişiklik olmamaktadır. Böylece embriyo inkübatör ortamında güvenli bir şekilde gelişimine devam ederken aynı zamanda da doktorunuz ve embriyologlar tarafından inkübatörden çıkarılmadan izlenebilmektedir.
Embriyo gelişimindeki ana olayların ve bunların uygun zamanda değerlendirilmesi ve kayıt altına alınması son yıllarda önem kazanmaktadır. Yumurta ve spermin birleşmesinden sonra döllenme, ilk ve sonraki hücre bölünmelerinin döllenme sonrası hangi saatlerde görüldüğü, hücre büyüklüklerinin karşılaştırılması, hücre içi organel dağılımları, morula ve blastosist oluşumları TLI ile klasik IVF laboratuvar uygulamalarına nazaran çok daha kesin bir şekilde tanımlanabilmektedir.
TLI'da her bir hastanın maksimum 12 embriyosunun aynı anda gerçek zamanlı ve geriye dönük karşılaştırmalı olarak izlenmesi mümkündür. Bu şekilde transfer öncesi son değerlendirmede doktorunuz ve embriyolog rahime tutunma olasılığı en yüksek olan embriyoyu en güvenilir şekilde seçebilmektedir. Ayrıca daha önce yavaş ve kötü embriyo gelişimi olan hastalarımızda bu durumun hangi evrelerden kaynaklandığı ve embriyo gelişimindeki problemin nasıl ortaya çıktığı ile ilgili çok değerli bilgiler edinebilmekteyiz.
Embriyonun rahime tutunması, embriyoyu çevreleyen glikoprotein yapısındaki zardan (zona pellucida) embriyonun dışarı tomurcuklanmasıyla (hatching) başlar. Tomurcuklanma embriyo gelişiminin 5. veya 6.günü blastosist aşamasına ulaştıktan sonra gerçekleşir. Embriyonun rahim içinde tutunabilmesi tamamıyla zardan çıktığında mümkün olmaktadır. Tüp Bebek için kullanılan ilaçların, embriyoyu çevreleyen zarı kalınlaştırdığı veya embriyoların içinde geliştirildiği kültür medyumlarının zarı sertleştirdiğini gösteren çalışmalar mevcuttur. Embriyoları dondururken ve çözerken kullanılan solüsyonlar da, embriyoyu çevreleyen zarın sertleşmesine neden olmaktadır. Bu nedenle embriyonun rahime tutunması zorlaşmaktadır. Embriyoloji laboratuvarında transfer öncesi embriyonun tomurcuklanmasını kolaylaştırmak amacıyla embriyoyu çevreleyen zarın inceltilmesi veya açılması (assisted hatching) işlemi uygulanmaktadır. Böylece kalınlaşmış veya sertleşmiş zardan(zona pellucida) embriyonun kurtulabilmesi kolaylaştırılır. Embriyoları çevreleyen zar belli bir bölgesinden inceltilir veya tam olarak açılır. Bu işlem embriyo transferi yapılacağı gün, transfer edilecek embriyolara uygulanır. Böylece embriyonun rahim duvarına tutunması kolaylaştırılır. Assisted Hatching (AHA) işleminde üç yöntem kullanılmaktadır.
Mekanik; cam mikroiğne ile embriyonun zarında açıklık meydana getirilir.
Kimyasal; Asit tyrode solüsyonu kullanılarak embriyoyu çevreleyen zar belli bölgesinden eritilerek inceltilir veya tam olarak açılır.
Lazer; Lazerle embriyonun zarı inceltilir veya açıklık oluşturulur. İşlem olarak en kısa sürede gerçekleştirilen ve en pratik olan yöntemdir.
Merkezimizde Lazer assisted hatching yöntemi kullanılmaktadır. Lazer asisted hatching yönteminin diğer yöntemlere göre tercih edilmesinin nedenleri şunlardır:
Embriyonun bulunduğu kültür ortamında, herhangi bir kimyasal kullanılmadan uygulanır.
İşlem olarak en kısa sürede gerçekleştirilen ve en pratik olan yöntemdir.
Lazer ile yapılan açıklık bilgisayar kontrollü ve mikrosaniye süreli olduğundan güvenlidir.
Embriyoyu ayrıca bir başka tutucu pipet ile tutmaya gerek kalmadan uygulanmaktadır.
Ayrıca embriyolara uygulanan genetik inceleme (PGT) için embriyodan bir hücrenin alınması amacıyla Lazer ile embriyonun dış zarına yapılan açıklık, bu işlemin kısa sürede ve pratik olarak yapılmasını sağlar.
Tekrarlayan tüp bebek uygulamalarında, kaliteli embriyo tranfer edilmiş olmasına rağmen gebeliğin elde edilememesi çoğunlukla implantasyon başarısızlığına bağlı olarak ortaya çıkmaktadır. Nedeni izah edilemeyen implantasyon başarısızlığı durumunda ve özellikle embriyoyu çevreleyen zarın kalın olduğu durumlarda assisted hatching işlemi implantasyon oranını artırmaktadır. AHA işlemi 2., 3. veya 4. gün transfer edilecek olan embriyolara uygulanmaktadır. AHA işlemi; 35 yaş üzerinde, FSH değeri normalin üstünde bulunan (FSH>10mlU/ml) kadınlarda, daha önceki uygulamalarında iyi kalitede embriyoların transferine rağmen gebelik gerçekleşmeyen olgularda, embriyo zarının kalın olması durumunda (>15µm) ve dondurulmuş çözülmüş embriyolarda dondurma solüsyonlarının embriyo zarını sertleştirmesi nedeniyle kullanılmaktadır.
|
|
|
|
Mekanik yöntem |
Asit yöntemi |
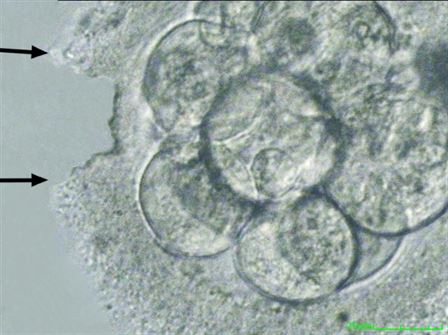
Lazer yöntemi (Merkezimizde Lazer assisted hatching yöntemi kullanılmaktadır)
|
|
|
Tomurcuklanma embriyo gelişiminin 5. veya 6.günü blastosist aşamasına ulaştıktan sonra
gerçekleşir. Embriyo zarının (Zona pellucida) erimesiyle tomurcuklanma başlar ve
embriyo tamamıyla zarından dışarı çıkar.
TRANSFER İŞLEMİ İÇİN EMBRİYO SEÇİMİ
Günümüzde mevcut değerlendirme yöntemleri embriyonun şekline veya hızlandırılmış video görüntüleri kullanılarak morfoloji ( şekle) ve morfokinetik (gelişime) görüntülere dayalı parametrelerle yapılmaktadır. Merkezimizde çok yakın bir zamanda uygulamaya girmiş olan tam otomatik ve standartlaştırılmış Artificial Intelligence (AI) olarak bilinen yapay zeka yöntemi çok sayıda embriyonun sürekli takip (TLI) sistemindeki ham video görüntülerini kullanarak eş zamanlı değerlendirmeyi amaçlayan üreme tıbbı alanındaki en yeni teknolojilerden biridir.
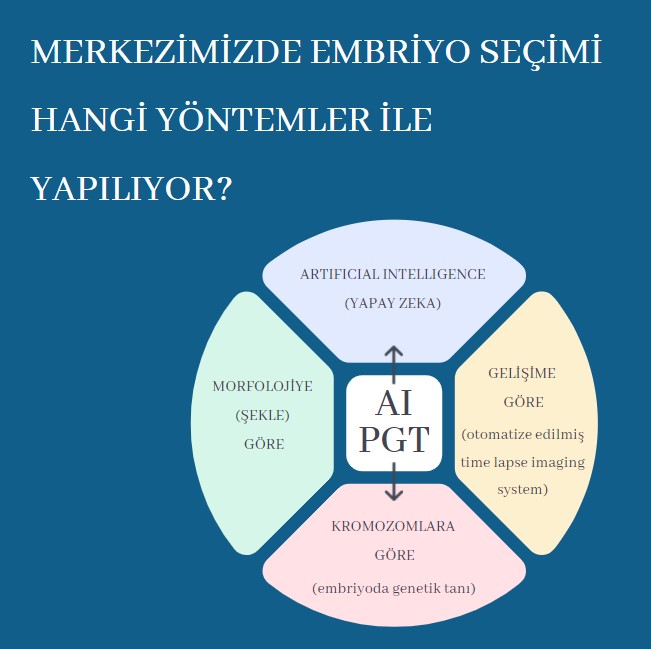
Tüp bebek (IVF) tedavilerinde çoğul gebeliklerin yenidoğan ve annede oluşturabileceği klinik komplikasyonlardan kaçınmak ve gebeliğe ulaşma süresini kısaltmak için implantasyon (tutunma) potansiyeli en yüksek embriyoların erken dönemde seçilmesi önemlidir. Bu amaçla merkezimizde transfer işlemi için her hastaya özel bireysel değerlendirme yapılarak en kaliteli ve tutunma potansiyeli en yüksek olan embriyonun seçiminde farklı embriyo seçim yöntemleri bir arada kullanılmaktadır.
1. Morfoloji ve Morfokinetik yöntemlerle (Time Lapse Imaging) embriyo seçimi;
Morfolojik Değerlendirme;
Merkezimizde implantasyon (tutunma) ve klinik gebeliğin birincil göstergesi olan blastokist kalitesi (5.gün embriyosu) morfolojik (şekilsel) olarak üç parametreyi içerisinde barındıran; Gardner ve arkadaşları tarafından oluşturan modifiye edilmiş sınıflama kullanılmaktadır. Bu sınıflamada embriyonun ekspansiyon (genişlik) oranı, ICM (iç hücre kitlesi) hücre sayısı ve yapısına göre kategorizasyonu, trofoektoderm (dış hücre kitlesi) hücre sayısı ve yapısına göre kategorizasyonu esasına dayanmaktadır.
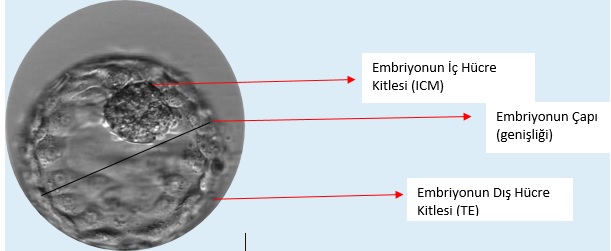
Morfokinetik Değerlendirmede,
Gelişim parametreleri olarak öncelikle bölünme zamanlamaları, fragmantasyon oranlari, blastomer boyutlari, doğrudan bölünmenin (direk klivaj) ve ters bölünmenin (reverse klivaj) etkileri incelenir.

2. Kromozomlara göre (Embriyoda Genetik Tanı, PGT) embriyo seçimi;
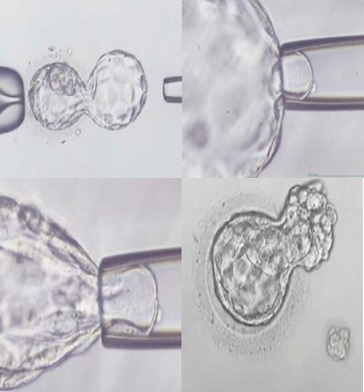
Trofoektoderm biyopsi işlemi sırasında embriyonun
trofoektoderm hücrelerinden 5-10 adet hücre alınması
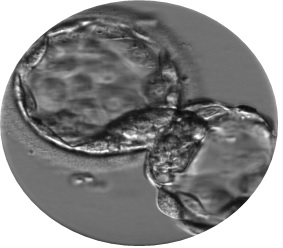
PGT sonrası kromozomları normal bulunan embriyo
3. Artificial Intelligence (Yapay Zeka) ile embriyo seçimi
Son yıllarda medikal pek çok alanda kullanımı yayınlaşmaya başlayan AI yöntemi IVF alanında da kullanılmaya başlanmıştır. Bir embriyoloğun değerlendiremeyeceği kadar çok sayıda veri setini aynı anda değerlendirebilen yapay zeka yöntemi ile tutunma potansiyeli en yüksek olan embriyonun seçimi konusunda IVF uzmanlarına rehberlik edecektir. Bir Deep Learning Machine (derin öğrenme) sistemi olan AI, embriyo gelişiminin değerlendirilmesinde kişilere bağlı değerlendirme farklılıklarını ortadan kaldırarak, tutunma şansı en yüksek olan embriyonun objektif olarak seçimine olanak tanır.
Farklı AI sistemlerinin geliştirilmesi ve bu çok yeni teknolojinin IVF sonuçlarına nasıl yansıdığı ile ilgili pek bilimsel yayın yapılmakta ve elde edilen sonuçlar bu teknolojinin embriyoları çok kısa sürede değerlendirerek tutunma potansiyeli yüksek embriyonun seçiminde daha yüksek başarı sağladığını (Kan-Tor ve ark. 2020), gebelik, implantasyon ve canlı doğum oranlarını arttırdığını (Tran ve ark. 2018; Friedenthal ve ark. 2021), genetik olarak normal (euploid) embriyonun PGT işlemine gerek kalmaksızın seçimine olanak sağlayabileceğini (Chavez-Badiola ve ark. 2020; Lee ve ark. 2021) göstermiş ve AI teknolojisinin IVF alanında potansiyel olarak başarı ile kullanılabileceğini ifade etmektedir.
Tek embriyo transferi ile canlı doğum oranlarını arttırmayı hedefleyen merkezimizde çok yakın bir zamanda kullanılmaya başlanan AI teknolojisi embriyoda genetik tanı yöntemleri ile birlikte kullanılarak tek embriyo transferinde en yüksek oranda ve en kısa sürede gebeliklerin elde edilmesi hedeflenmektedir.
EMBRİYO TRANSFERİ
Başarılı Sonuç İçin Başarılı Embriyo Transferi Şart
Tüp bebek tedavisinin son basamağı olan embriyo transferi önemli bir işlemdir. Ortalama olarak bir aya yakın süren tedavi sonucu geliştirilen embriyolar artık hastaya bu işlem ile transfer edilecektir. Embriyo transferinde temel prensip, embriyoların rahim içinde belirlenecek bölgeye mümkün olduğunca en az travma ile yerleştirilmeleridir. Uygun şartlarda yapılan embriyo transferi, tüp bebek tedavisinde başarıyı arttıran bir faktördür ve önemi göz ardı edilemez. Bu nedenle transferi gerçekleştirecek doktorun ve embriyoloğun dikkati, özeni ve sabrı büyük önem taşımaktadır. Kullanılan kateter tipi ve transfer yapma tekniği de başarıda etkili diğer unsurlardır.
Transfer Edilecek Embriyo Sayısı Nasıl Belirlenmektedir?
Transfer edilecek embriyo sayısı belirlenirken hem yüksek gebelik oranlarının elde edilmesi hedeflenmekte hem de çoğul gebelik riskinin mümkün olabilecek en az düzeyde olması amaçlanmaktadır. Embriyo seçim kriterlerinin yetersizliği nedeniyle tüp bebek tedavisinin yapılmaya başlandığı ilk yıllarda çok sayıda embriyo transfer ediliyordu. Ancak zamanla yüksek teknolojik donanıma sahip merkezlerde, deneyimli ekiplerce seçilen protokol ve ilaçların en uygun dozlarda kullanımı, embriyoların doğal ortama yakın şartlardaki kültür ortamlarında geliştirilmeleri, embriyoların seçim kriterlerinin daha iyi belirlenmesi ve özellikle blastosist dönemindeki embriyoların transferi rahime tutunma oranlarını arttırmıştır. Transfer edilecek embriyo sayısı kadın yaşı ve daha önce uygulanan başarısız tüp bebek denemeleri göz önüne alınarak, gelişen embriyoların kalitesi ve dönemine göre seçilmektedir. Merkezimizde transfer işlemi yapılmadan önce aileler ile görüşülerek bilgilendirme yapılmakta ve çoğul gebeliğin oluşturacağı riskler anlatılarak mümkün olduğunca iyi ve az sayıda embriyonun transferinin yapılması önerilmektedir. Merkezimizde uyguladığımız embriyo transfer stratejisi, blastosist (5. gün) düzeyine ulaşmış elektif tek embriyonun rahim içine verilmesidir. Böylece ikiz ve üçüz gebelikler dramatik olarak azaltılmaktadır. İleri kadın yaşı ve tekrarlayan başarısız denemeleri olan çiftlerde ve dondurulmuş çözülmüş embriyo taransferi yapılan çiftlerde, transfer öncesi embriyonun dış çeperi olan zona pellucida'nın lazer ile inceltilmesi veya tam açıklık yapılması işlemi uygulanır. Bu işlem AHA(Assisted Hatching-yardımcı yuvalama) olarak adlandırılmakta ve embriyonun zonadan ayrılmasını kolaylaştırarak implantasyon şansını olumlu etkilemektedir.
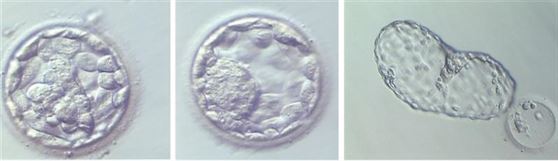
Blastosist dönemindeki embriyolar
İlk Muayenede Kateter Provası Yapılıyor
Embriyo transferinin kolay yapılması amacıyla hastanın ilk muayeneye geldiği gün kateter ile transfer provası yapılmakta ve böylece muhtemel zor transferler için önlem alınmaktadır. Geçirilmiş cerrahi veya elektrokoter uygulamalarına bağlı olarak rahim ağzında daralma veya yer değiştirme oluşmuş olabilir. Bunun yanı sıra miyom basısı veya doğumsal anomali gibi nedenlerle de embriyo transferi zor olabilir. Histeroskopik olarak incelenmesi ve problem saptanırsa düzeltilmesi sağlanmaktadır.

Transfer katateri
Embriyolar Ultrason Rehberliğinde ve Dolu Mesane İle Transfer Ediliyor
Embriyoların rahim içinde verileceği en uygun yerin tespit edilmesi ve rahim içi zarına dokunulmaması açısından embriyo transfer işleminin dolu mesane (idrar torbası) ile ultrasonografi eşliğinde yapılması tercih edilmektedir. Bu şekilde rahim ağzı ve rahim arasındaki açı tespit edilerek transfer kateterinin izleyeceği yol belirlenmekte ve işlemin daha az travmatik olması sağlanmaktadır. Yüksek çözünürlüğü olan ultrason kullanımı da transfer işleminin daha iyi görülmesini sağlayarak başarıyı olumlu etkilemektedir. Mesanenin dolu olması transfer işlemini kolaylaştırmaktadır. Rahimin öne doğru bir eğimi varsa rahim ve rahim ağzı arasındaki açıyı azaltmakta böylece rahimi düzleştirerek transfer kateterinin geçişini kolaylaştırmaktadır.
|
|
|
|
Embriyo transfer işleminin Ultrasonografik (USG) görüntüsü |
|
Embriyo Transfer İşlemi Ağrısızdır ve Anestezi Gerektirmez
Transfer işlemi sırasında rahim ağzında bulunan mukus steril bir çubuk ile temizlenir, ince ve yumuşak bir kateter yardımı ile embriyolar rahim içerisine bırakılır. Transferde yumuşak kateter tercih edilmesi, rahim ağzında kanama riskini de azaltmaktadır. Kullandığımız kateterlerin uçları ultrasonla gözlenebildiği için embriyoların rahim içinde bırakılacağı bölge net olarak tespit edilebilmektedir. Embriyolog tarafından doktor ile eş zamanlı olarak uygun koşullarda katater içerisine yüklenen embriyoların transferi nazik bir şekilde yapıldıktan sonra kateter yavaşça çıkarılır ve embriyolog tarafından mikroskop altında bakılarak embriyoların tümünün transfer edildiği kontrol edilir.
Transfer Sonrası Uzun Süreli Yatak İstirahatı Gebelik Şansını Artırmaz
Embriyolar rahime yerleştirildikten sonra yarım saatlik dinlenme yeterlidir. Daha uzun süreli yatak istirahatının gebelik şansını arttırıcı etkisi olmadığı saptanmıştır. Hastalarımıza ilk 24 saatte fiziksel aktiviteden kaçınmalarını öneriyoruz. Daha sonraki gün ise normal yaşama dönülmesi mümkündür, hasta çalışıyorsa işine devam edebilir. Embriyo transferi sonrası transfer gününe göre 9 ila 11. günler arası verilen yazılı formda belirtile tarihte kanda gebelik testi yaptırılır. Gebelik sonucunu alıncaya kadar spor, ağır iş, ağır yük kaldırma gibi aktivitelerden kaçınılmasını öneriyoruz. Araba ve uçak yolculuğu ise yapılabilir. Seyahat edilmesinde sakınca bulunmamaktadır.
Embriyo Transferi
PGT (Preimplantasyon Genetik Tanı)
Preimplantasyon Genetik Tanı Uygulamasında Polar Hücre Biyopsi Yöntemi
Polar hücreler yumurta hücresinin olgunlaşması ve döllenmesi sonrasında atılan yan ürünlerdir. Embriyolardaki kromozomal sayı anomalilerinin büyük çoğunluğu yumurta hücrelerinin oluşumu sırasında gerçekleşmektedir. IVF tedavisine giren 35 yaş ve üzeri kadınlarda 1. ve 2. polar hücrelerin analizi sonrasında incelenen yumurtaların yarısından fazlası kromozomal bozukluk taşır. Özellikle Down Sendromlu bebek dünyaya getirme sıklığı 35 yaş ve üzeri kadınlarda oldukça hızlı bir artış gösterir. Bu nedenle polar hücrelerin kromozomal olarak incelenmesi, ileri yaşta az sayıda yumurtası olan anne adaylarında anneden kaynaklanan kromozomal problemlerin tanısında önemli bir yere sahiptir.
Preimplantasyon genetik tanı (PGT), embriyoların anne rahmine yerleştirilmeden önce genetik açıdan ve kromozomlar yönünden incelenmesi işlemidir. Embriyolar 8 hücreli olduktan sonra laboratuvarda biyopsi ile alınan bir hücreye uygulanan genetik analiz, anneye sağlıklı embriyonun transfer edilmesine yardımcı olur. Özellikle ileri anne yaşı (38 yaş ve yukarısı) söz konusu olduğunda anneden gelen kromozomlarda bozukluklar olmakta dolayısıyla embriyolar şekil ve yapı itibariyle normal görünseler bile kromozom anomalilerine bağlı olarak gebelik gelişmemekte veya gelişen gebelik düşükle sonlanabilmektedir. Yapılan araştırmalarda iyi kalitede görünen embriyolarda hemen hemen % 38–40, kötü kalitedeki embriyolarda % 90’lara varan oranlarda kromozomal bozukluk saptanmıştır. PGT’nin amacı kromozomal anormallikler açısından en az riskli olan embriyoların seçiminin sağlanmasıdır. PGT; ileri anne yaşı yanı sıra tekrarlayan düşükleri olan vakalarda, tekrarlayan başarısız tüp bebek denemesi olan çiftlerde, şiddetli erkek infertilitesi olan vakalarda, genetik hastalık riski taşıyan vakalarda uygulanmaktadır. PGT ile kromozomal anormalliklerin saptanmasının avantajları; embriyonun rahim içine tutunması ve gebelik şansının artması, düşük riskinin azalması, kromozomal açıdan normal bir bebek sahibi olma şansının artmasıdır. Diğer yandan ağır erkek kısırlığı ile başvuran çiftlerde altta yatan sebebin yüksek oranda genetik kaynaklı olduğu gözlenmektedir. Bu çiftlerde de öncelikle erkeğin spermlerinde genetik analiz yapılarak durumun saptanması ve ardından embriyolarda genetik tanı yapılarak sağlıklı embriyoların transferi gebelik şansını önemli oranda arttırmaktadır.
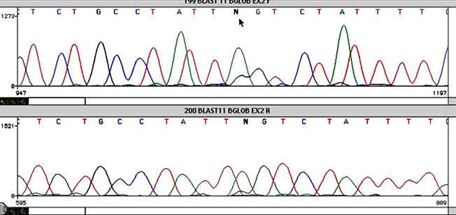
PGT uygulamasından yarar sağlayacak bir diğer hasta grubu da Talasemi ( Akdeniz Anemisi), Kistik Fibroz, Ailevi Akdeniz Ateşi ve bunun gibi kalıtsal hastalık taşıyıcı bireylerdir. Özellikle her ikisi de Talasemi taşıyıcısı olan çiftlerden hastalıklı çocuk doğma olasılığı % 25 olup bu hastalık ömür boyu tedavi gerektiren, sürekli kan nakillerine gereksinim duyulan, iyi tedavi edilmediği takdirde hastaların erken yaşlarda kaybedildiği ciddi bir durumdur. Taşıyıcı olduğu bilinen çiftin gebelik öncesi genetik tanı yöntemleri ile sağlıklı çocuk dünyaya getirmesi sağlanabileceği gibi taşıyıcı olduğunu ancak hastalıklı bir çocuğa sahip olduktan sonra öğrenen çiftlerde de yine bu yöntemle doku tipi uyumlu bir bebek dünyaya getirilerek bu bebeğin kordon kanından veya kemik iliğinden yapılacak nakil ile hastalıklı kardeşte tam şifa sağlanabilmektedir. Unutmamalıdır ki talasemi taşıyıcılığı yurdumuz genelinde %4,5 oranında görülürken Akdeniz ve Trakya bölgelerinde bu oran %12 civarına çıkabilmektedir.
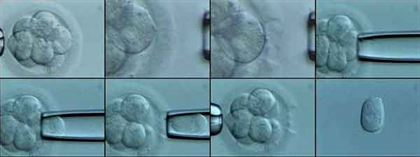
Preimplantasyon Genetik Tanı Uygulamasında Trofektoderm Biyopsi Yöntemi
Tüp Bebek tedavisiyle oluşturulan embriyolar anne rahmine yerleştirilmeden önce genetik açıdan incelenebilir. Böylece sağlıklı embriyonun seçimi gerçekleştirilir.
Genetik hastalıkların tanımlanması ve HLA uyumlu embriyonun seçimi amacıyla embriyo gelişiminin 3. veya 5. günlerinde uygulanan biyopsi işlemi ile alınan hücreler genetik laboratuvarında PCR yöntemi ile analiz edilirler. PCR yöntemi alınan her bir hücredeki DNA materyalinin başarılı bir şekilde çoğaltılması esasına dayanır. 3. günde 6-8 hücre (blastomer) içeren embriyodan yalnızca bir hücre alınarak PCR işlemi uygulanabilirken 5. günde blastosist gelişimi gösteren embriyonun trofektoderm hücrelerinden 5-6 hücre alınarak PCR yöntemi ile daha güvenilir sonuçlar elde edilebilmektedir.
Laboratuvarda uygun kültür ortamında 5. günde blastosist aşamasına gelen embriyolara preimplantasyon genetik tanı amacıyla biyopsi işlemi uygulanmaktadır. Blastosist aşamasındaki embriyonun trofektoderm hücrelerinden plasenta, iç hücre kitlesinden ise fetüs (bebek) gelişmektedir. Blastosist aşamasında embriyonun toplam hücre sayısı yaklaşık 40-150’dir. Blastosist biyopsisinde yalnızca trofektoderm hücrelerinden 5–6 hücre alınarak iç hücre kitlesine dokunulmaz. Biyopsi ile alınan hücre sayısı arttığı için genetik incelemede tanı koyma başarısı yükselir.
Embriyo gelişiminin 3. gününde embriyonun dış zarında (zona pellucida) lazer ışınları gönderilerek küçük bir açıklık oluşturulur. 5. veya 6. günde açılan açıklıktan mikro düzeyde ince cam biyopsi pipetiyle 5–6 trofektoderm hücresi blastosistten biyopsi yolu ile ayrıştırılır. Alınan bu hücreler genetik hastalık yönünden sağlıklı ve/veya hasta kardeş ile doku uyumu olan embriyonun seçilmesi amacı ile genetik laboratuarına verilirken embriyo gelişimi laboratuar koşullarında devam ettirilir. 24–48 saat süren yoğun genetik testler sonuçlanır. Belirlenen uygun embriyolar anne adayının rahim içine transfer edilir.
İlk kez ekibimiz tarafından Akdeniz anemisi hastalığına sahip bir çocuğu olan ailede tüp bebek yöntemiyle elde edilen embriyolardan, hasta çocukla aynı doku tipi ile uyumlu olan sağlıklı embriyolar, trofektoderm biyopsi yöntemi uygulanarak seçilmiş ve gebelik elde edilmiştir.
|
|
|
|
Biyopsi öncesi blastosist aşamasındaki embriyo |
Embriyo holding pipetle tutulur |
|
|
|
|
5-6 trofektoderm hücresi biyopsi pipeti ile aspire edilir. |
|
|
|
|
|
Lazer ışınları yardımı ile trofektoderm hücreleri blastosisten ayrıştırılır |
Lazer ışınları yardımı ile trofektoderm hücreleri blastosisten ayrıştırılır |
EMBRİYO DONDURULMASI (VİTRİFİKASYON)
Embriyo dondurma işlemi, embriyo transferi sonrası kalan embriyolardan uygun kalitede olanların özel bir hazırlık işlemine tabi tutulduktan sonra sıvı azot içerisinde saklanmasıdır.
Tüp bebek denemesinde gebelik elde edilememesi, gebelik elde edilip düşükle sonlanması ya da doğumla sonlanan bir gebelikten sonra çiftin tekrar bir bebek dünyaya getirmeye karar vermesi durumunda daha önce kendi sperm ve yumurta hücrelerinin döllenmesiyle elde edilen ve dondurulan embriyoları çözülüp kadın rahmine yerleştirilerek gebelik sağlanabilir. Bu yöntemle kadına uzun süren hormon ilaçlarının verilmesi engellendiği gibi tüp bebek işlemindeki gerekli birçok aşama atlanacağı için maliyet bakımından da çiftlere kolaylık sağlamaktadır. Merkezimizde embriyo dondurma teknikleri ile elde edilen sağlıklı gebelik oranı % 38 ile 40 oranındadır.
Embriyoların dondurulması çeşitli nedenlerden dolayı zorunlu olarak da yapılmaktadır. Embriyoların transfer edileceği dönemde kadına ait herhangi bir sorun ortaya çıkması durumunda (örneğin hormon tedavisi sırasında yumurtalıkların aşırı uyarılması, OHSS) tüm embriyolar dondurulup kadında hayati risk oluşturan bu tablonun gerilemesinden sonra daha emniyetli bir zamanda çözülerek transfer edilebilirler. Yine rahim içi zarının (endometriyum) kalınlığının gebelik için yeterli olmaması durumunda da embriyolar dondurularak saklanıp endometriyum gelişiminin yeterli olduğu başka bir dönemde çözülerek transfer edilebilirler.
Embriyolar 1.günden 6. güne kadar gelişimlerinin her aşamasında dondurulabilmektedir. Ancak çözme sonrası en yüksek sayıda canlı embriyo elde edilebilmesi için dondurma işleminin embriyoların gelişim aşamasına özel bir teknikle uygulanması gerekmektedir. Embriyo transferi sonrası kalan sağlıklı embriyoların dondurulması için Türkiye’de ilk olarak merkezimizde gerçekleştirilen başarısı klinik deneyler ile ispatlanmış olan embriyo vitrifikasyonu, bir başka ifade ile camsılaştırma, yöntemi kullanılmaktadır. Vitrifikasyon yönteminin en önemli özelliği, embriyoların yüksek yoğunluktaki koruyucu madde ile 3–4 dakika muamele edildikten sonra dakikada eksi 2000–20.000 santigrad derece soğutma hızı ile hasar görmeden dondurulabilmesine imkan sağlamasıdır. Klasik-yavaş embriyo dondurma yönteminin aksine, vitrifikasyon veya hızlı dondurma yöntemi ile özellikle 3. ve 4. gün ve blastosist dediğimiz 5. ve 6. gün embriyoları çok daha başarılı bir şekilde dondurulmaktadır. Dondurma yönteminin başarısını gösteren en önemli kriterleden biri olan çözme sonrası embriyolardaki canlılık oranı, vitrifikasyon ile dondurulup çözülmüş olan embriyolarda neredeyse %100’e yakındır. Embriyo çözme sonrası yüksek canlılık oranına ilave olarak vitrifikasyon yöntemi, anne adaylarına tekrar ve yüksek gebelik şansı veren en başarılı dondurma yöntemidir.
Merkezimizde embriyo dondurma teknikleri ile elde edilen sağlıklı gebelik oranı % 50-60 oranındadır.
Embriyo dondurma işlemi
|
|
|
|
|
|
Embriyo dondurma (Vitrifikasyon) |
|||
|
|
|
|
|
|
Embriyo çözme |
|||
|
|
|
|
|
Dondurulmuş embriyoların saklandığı sıvı azot tankları (-196 ºC) |
||
OVER DOKUSU DONDURULMASI VE TRANSPLANTASYONU
Günümüzde, gelişen tedavi yöntemleri ile birçok kanser türünde kür sağlanabilmektedir. Bu sevindirici ilerlemelere rağmen bu tür tedaviler sonrasında birçok genç kadın hayatının geri kalan kısmını infertil olarak geçirmekte ve erken dönemde menopozla karşı karşıya kalmaktadır. Aynı problem çocukluk yaşı tümörleri, rahim kanseri gibi erken yaşta herhangi bir nedenle yumurtalıkları ameliyat ile alınmış kadınlar için de geçerli olmaktadır. Böyle durumlarda, yumurtalıkların veya yumurtalıklardan alınan bir parçanın, çeşitli koruyucu maddeler içerisinde dondurularak saklanması işlemi merkezimizde uygulanmaktadır. İşlemde yumurtaları içeren yüzey dokusundan bir örnek alınır, küçük parçalar halinde dondurularak saklanır. Dondurulan dokular daha sonra çözülerek kullanılmak üzere -196⁰C'de sıvı azot tanklarında saklanır. Over dokusunun dondurulup çözüldükten sonra tekrar vücuda yerleştirildiğinde fonksiyonlarını koruduğu gözlenmiştir. Bu yöntem yumurtalık kapasitesini erken yaşta kaybetme riski ile karşı karşıya kalan kadınlar için bir ümit oluşturmaktadır.

Over dokusu dondurma işlemleri
LABORATUVAR KALİTE KONTROLÜ
BOOMERANG WiLOGICAL Dış Kalite Kontrolü;
Boomerang WiLOGICAL, IVF kliniklerinde kalite güvence çalışmalarını sürdürebilmek için özel olarak tasarlanmış kablosuz bir kayıt ve alarm sistemidir. Boomerang WiLOGICAL, belirlenen süre aralığı içerisinde kritik parametreleri sürekli olarak kontrol ederek kayıt altına alır. Bu izlenebilirlik ve güvenlik GLP, GMP ve FDA CFR21 part II kalite sertifikalarına göre geliştirilmiştir. IVF kliniğinde kullanılan, içerisinde embriyoların geliştirildiği inkübatörlerin anne rahmini taklit etmesi prensibine göre, sıcaklık, nem, CO2 ve O2 değerlerinin çok hassas olarak belirli değerlerde sürekli olarak sağlanması gerekmektedir. Boomerang sistemi ile belirlenen parametreler ölçülür ve kayıt altına alınır. IVF kliniğinde kullanılan eksi 196°C derin dondurucular olan kriyojenik tanklar (sıvı azot tankları ve buhar fazlı tanklar) sıcaklık değerlerini belirlenen düzeylerde takip ederek kritik ısı değişikliklerini belirlenen zaman dilimi içerisinde kayıt alır. Boomerang WiLOGICAL, sisteme tanımlı kullanıcılara gerçek zamanlı alarmları (SMS) gönderir ve web tabanı üzerinden sürekli erişilebilirlik sağlar. Bu özellikler sayesinde IVF hastalarının embriyo, sperm, oosit gibi dondurulmuş örnekleri daha güvenle saklanmakta ve gelişimleri takip edilen embriyolarının içinde bulunduğu inkübatörler ve laboratuvardaki tüm ısıtıcı yüzeylerinin sürekli kalite kontrolü sağlanmış olacağından laboratuvar başarı oranları artmaktadır. Bu sistemle kontrol edilen parametreler özetle;
İnkübatör karbondioksit,oksijen ve sıcaklık değerleri
İnkübatör kapak açılış-kapanışları
Laboratuvar kapı açılış-kapanışları
Laboratuvar içi sıcaklık,nem ve karbondioksit
Oda basınçları
Buzdolabı sıcaklıkları
Kriyotank sıvı nitrojen seviyeleri
İnkübatör karbondioksit,oksijen ve sıcaklık değerlerinin takibi, embriyo kültürünün yapıldığı inkübatörlerde embriyoların içinde bulunduğu kültür sıvısının embriyo için uygun olan asitlik derecesine ve sıcaklığının istenen koşullarda tutulduğunun kontrolü açısından önemlidir.
İnkübatör kapak açılış-kapanışlarının takibi hem inkübatör kapağının yanlışlıkla açık bırakılmasını önlemekte hem de bu verilerin inkübatörler arasındaki farklılığını görerek laboratuvarda bulunan vakaların inkübatörler arasında eşit olarak dağıtılmasını sağlaması açısından önemlidir. Böylece bir inkübatöre diğerlerinden fazla vaka konularak o inkübatörün koşullarının gereksiz yere etkilenmesi engellenmiş olur.
Laboratuvar kapı açılış-kapanışlarının ve oda basıncının takibi laboratuvar giriş-çıkış sıklığının ölçülebilmesi ve laboratuvar havasının sterilizasyonunun korunması için gerekli olan pozitif oda basıncının (laboratuvara dışarıdan hava girişini engelleyen basınç farkı) korunmasını sağlamak bakımından önemlidir.
Laboratuvar içi sıcaklık, nem ve oksijen değerlerinin takibi, bu değerlerin değişiminden etkilenebilecek, başta inkübatörler olmak üzere, cihazların korunması, hücrelere inkübatör dışında uygulanan işlemlerde (yumurta toplama,mikroenjeksiyon,embriyo değerlendirmesi vs.) uygun koşullarda çalışılması ve laboratuvar personelinin çalışma koşullarının uygunluğunun kontrolü bakımından önemlidir.
Buzdolabı sıcaklıklarının takibi, bu cihazlar içerisinde saklanan başta kültür sıvıları olmak üzere laboratuvar kimyasallarının uygun koşullarda saklandığının kontrolü bakımından önemlidir.
Kriyotank sıvı nitrojen seviyelerinin kontrolü, bu tanklar içerisinde saklanan ve canlılıklarının korunabilmesi için sıvı nitrojen(-196°C) içerisinde bulunması gereken embriyo, sperm ve over dokularının güvenliği bakımından önemlidir.
Sonuç olarak bu sistem sayesinde mesai saatleri dışındaki zamanlarda dahil olmak üzere hastalarımızın laboratuvarımıza emanet etmiş olduğu hücrelerin en iyi koşullarda işlem gördüğü ve saklandığı garanti edilmiş olmaktadır.
|
|
||
|
|
||
|
Boomerang dış kalite kontrol sistemiyle inkübatörkerin ısı ve ortam özellikleri, sıvı ve buhar fazlı azot tanklarının -196 derecelik ısılarının kontrolü, medikal buzdolapları ve işlemlerin yapıldığı yüzey ısılarının sürekli kontrolleri yapılabilmektedir. |
|
|
RI WITNESS SİSTEMİ
Tüp Bebek tedavisi için merkezimize başvuran hastalarımızın, sıklıkla sorduğu konulardan bir tanesi de sperm, embriyo ve yumurtaların karışmasının önlenmesine yönelik laboratuvarda nasıl bir önlem alındığı sorusudur. Mayıs 2019 tarihine kadar; çiftlere ait sperm kapları, yumurta ve embriyoların saklandığı kültür kapları ve dondurma işleminde kullanılan taşıyıcıların üzerine çiftlerin protokol numaraları, ad/soyadları, işlem tarihlerinin kaplar üzerine yazılması ve bunun işlemi yapan kişi dışında ikinci bir laboratuvar çalışanı tarafından kontrol edilmesi ile bu önlemler alınmaktaydı. 22 Mayıs 2019 tarihinden itibaren bu önlemlere tüm aşamaları elektronik olarak kontrol eden radyofrekans tabanlı RI Witness sistemi de eklenmiştir. Bu sistem çiftlerin sperm ve yumurta örneklerinin laboratuvar ortamına alınmasından önce başlar. Örneklerin bulunduğu ve işlemlerin yapıldığı tüm kaplara özelleşmiş mikroçipler takılarak, laboratuvar süreçlerinde yapılan tüm işlemleri, uygulayan kişi, yapılan işlemin tarih ve saati, işlemi kontrol eden 2. kişinin kim olduğu gibi birçok parametre ile elektronik ortamda kontrol eder ve kayıt tutar. Ayrıca embriyo, sperm yumurta dondurulması işlemlerinde -200 C ye dayanıklı özel üretilmiş barkodlar kullanılarak tüm süreçler güvence altına alınır. Kısaca bu sistem, çifte ait gametler (yumurta, sperm) ve embriyolar laboratuvar içinde bir kaptan veya tüpten diğerine her taşındığında insan hatası riskini azaltmaya yardımcı olur ve tüp bebek döngüsünün her basamağını korur.

Sistemin çalışma prensipleri:
1. Siklus Başlangıcı: Tüp bebek tedavisi başlayan her çifte kişiye özel bir RFID kimlik içeren kart tanımlanır. Çiftten bu kartı yumurta toplama ve embriyo transfer aşamalarında ibraz etmeleri istenir. (Şekil1).
Şekil 1
2. Yumurta Toplama ve Sperm Verme: RI Witness etiketler örneklerin bir kültür kabından diğerine alındığı işlem adımlarını kimliklendirme, izleme ve kayıt imkanı verir (Şekil 2).
Şekil 2
3. Uyumsuzluk: Başka bir hastanın örneği aynı çalışma alanında çalışılamaz. Çalışma alanında farklı kimlikte bir örnek algılandığı an RI Witness alarm uyarısı devreye girer (Şekil 3).

Şekil 3
4. İnseminasyon: RI Witness örnek kimliklerini doğruladıktan sonra bir sonraki adıma geçmeye izin verir (Şekil 4).

Şekil 4
5. Embriyo Kültürü: Embriyonun durumu, son aktivitesi ve embriyolog kimliği kültür kabı çalışma alanına getirildiği an sistemde görünür (Şekil 5).

Şekil 5
6. Biyopsi: Embriyo transferi, biyopsi işlemi ya da vitrifikasyon işlemlerinde de RI Witness izleme ve takibe devam eder (Şekil 6).

Şekil 6